


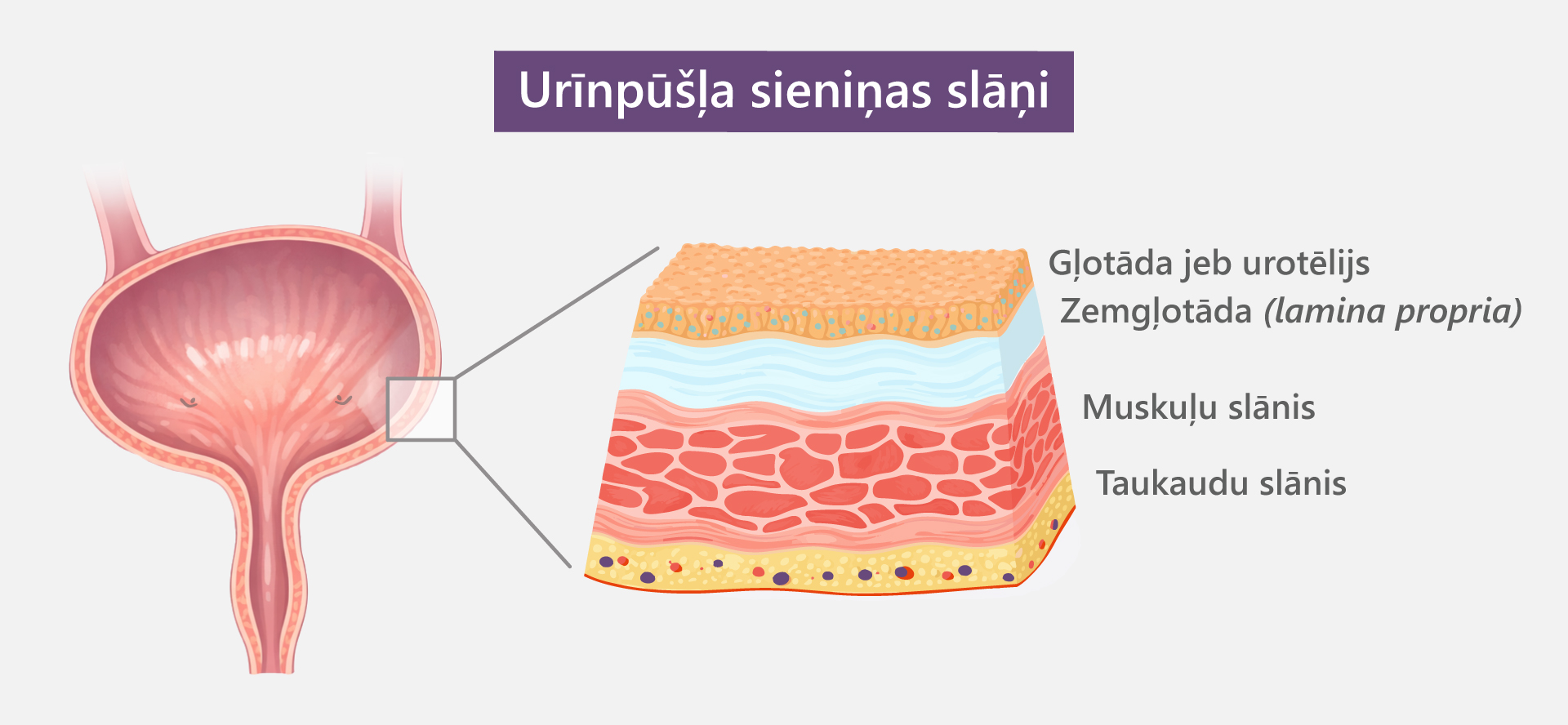
Urīnpūslis ir orgāns, kas uzkrāj nieru ražoto urīnu, tālāk to izvadot no ķermeņa caur urīnizvadkanālu. Urīnpūšļa sieniņai ir četri slāņi: gļotāda urīnpūšļa iekšpusē jeb urotēlijs, zem gļotādas esošais lamina propria jeb saistaudu slānis, muskuļu slānis un taukaudu slānis, kas atdala urīnpūsli no citiem orgāniem.

Urīnpūšļa vēzis sākas, kad urīnpūšļa iekšpusi klājošās gļotādas jeb urotēlija šūnas kļūst patoloģiskas un sāk nekontrolēti augt un dalīties. Galvenie šī vēža attīstības riska faktori ir smēķēšana, kas izraisa aptuveni pusi no visiem saslimšanas gadījumiem, kā arī noteiktas ķīmiskās vielas, jonizējošais starojums un biežas urīnceļu infekcijas, lai gan vēzis var attīstīties arī bez riska faktoru klātbūtnes.
Urīnpūšļa vēzis ir septītais vīriešu vidū izplatītākais vēža veids un desmitais izplatītākais, ja saslimstības statistikā ņem vērā abus dzimumus.1 Tas biežāk sastopams vīriešiem nekā sievietēm, un tā sastopamība palielinās līdz ar vecumu – visbiežāk to atklāj cilvēkiem pēc 75 gadu vecuma.2
Urīnpūšļa iekšējais slāni veido gļotāda – lielākā daļa urīnpūšļa vēža gadījumu sākas tieši gļotādas šūnās. Šo vēža veidu sauc par uroteliālo karcinomu. Taču retos gadījumos urīnpūšļa audzējam ir citu veidu šūnu pazīmes, un tādos gadījumos urīnpūšļa vēža apakštips ir cits. Nākamie izplatītākie urīnpūšļa vēža apakštipi ir plakanšūnu karcinoma un adenocarcinoma.
• Plakanšūnu karcinomas attīstība sākas urīnpūsli izklājošajās plakanajās šūnās un veido aptuveni 5 % no visiem urīnpūšļa vēža gadījumiem.3
• Adenokarcinomas attīstība sākas urīnpūsli izklājošajās dziedzeršūnās un veido 1-3 % no visiem urīnpūšļa vēža gadījumiem.4
Pārējie apakštipi (sarkoma, sīkšūnu karcinoma un citi) ir sastopami vēl retāk. Parasti šo apakštipu ārstēšana sākotnējās stadijās līdzinās tipiskai urotēlija karcinomas ārstēšanai. Tomēr daži apakštipi var attīstīties vai progresēt ātrāk nekā urotēlija karcinoma, un tādos gadījumos parasti nepieciešama agresīvāka ārstēšanas taktika. Šajā materiālā galvenā uzmanība pievērsta uroteliālajai karcinomai.

Visbiežākais un bieži vien agrākais urīnpūšļa vēža simptoms ir asinis urīnā jeb hematūrija, kas parasti izpaužas kā sārts vai sarkans urīns (makrohematūrija jeb ar aci saskatāma asiņu klātbūtne urīnā), tomēr dažreiz konstatējama tikai ar mikroskopu (mikrohematūrija).

Šos simptomus var izraisīt arī citi iemesli, piemēram, urīnceļu infekcijas – lai noteiktu to patieso cēloni, vienmēr jāvēršas pie ārsta. Turklāt jāpatur prātā, ka dažreiz urīnpūšļa vēzim var nebūt nekādu simptomu.

Riska faktori ir personīgi, dzīvesveida, vides vai iedzimtības aspekti, kas palielina iespēju saslimt ar kādu slimību, šajā gadījumā ar urīnpūšļa vēzi. Riska faktori var būt gan ietekmējami jeb modificējami, gan neietekmējami jeb nemodificējami. Parasti vēzis attīstās, pastāvot vairāku riska faktoru kombinācijai.


Urīnpūšļa vēža agrīnai atklāšanai šobrīd nepastāv valsts mēroga, plašai populācijai paredzētas skrīninga programmas. Lielākā daļa gadījumu tiek atklāti, kad pacients vēršas pie ārsta ar sūdzībām par simptomiem (visbiežāk asinīm urīnā), vai arī audzējs tiek atklāts nejauši, veicot izmeklējumus citu veselības traucējumu dēļ. Bieži vien sākuma stadijās šis vēzis var izraisīt maz simptomu vai neizraisīt tos vispār, tādēļ svarīgi vienmēr laikus griezties pie ārsta, ja parādās neparasti ar urīnceļiem saistīti simptomi. Urīnpūšļa vēža diagnoze tiek noteikta, balstoties vairāku izmeklējumu rezultātos.

Pastāvot aizdomām par urīnpūšļa vēzi, ārsts vispirms iztaujās par pacienta veselības stāvokli, pievēršot uzmanību urīnceļu darbībai, iepriekšējām urīnceļu infekcijām, akmeņiem urīnvados vai urīnpūslī, agrāk veiktām uroloģiskām procedūrām, smēķēšanas vēsturei un iespējamai saskarei ar ķimikālijām darbā, kā arī citām slimībām (tostarp arī ģimenes saslimšanu vēsturei) un lietotajiem medikamentiem. Pēc tam ārsts var pārbaudīt ķermeņa temperatūru, asinsspiedienu, sirdsdarbības ātrumu un elpošanu, iztaustīt vēderu, iegurni un dzimumorgānus.15
Biomarķieri ir bioloģiskas molekulas, kas var liecināt par vēža klātbūtni organismā. Tās ražo vai nu pats audzējs, vai organisma veselās šūnas, reaģējot uz audzēju. Biomarķieru testi, tāpat kā visi pārējie izmeklējumi, palīdz izvēlēties vispiemērotāko ārstēšanas veidu un taktiku. Vienlaikus jāatceras, ka biomarķieru līmeni var ietekmēt arī ar audzēju nesaistīti procesi.
Urīnpūšļa vēža gadījumā biomarķieru testus izmanto specifisko gadījumos, piemēram, lai novērotu, kā uz ārstēšanu reaģē muskuļus neinvadējoši urīnpūšļa audzēji. Latvijā biomarķieru testus šī vēža diagnostikā neizmanto.
Tie visbiežāk ir vieni no pirmajiem izmeklējumiem, ko veic, ja ir aizdomas par urīnpūšļa vēzi. Ķermenī tiek ievadīta plāna, elastīga caurulīte, kurai piestiprināta kamera. Projicējot attēlu uz ekrāna, iespējams apskatīt orgāna iekšpusi.

Vēža stadija atspoguļo to, cik tālu un cik ātri vēzis ir izplatījies. Šī informācija nepieciešama, lai prognozētu slimības gaitu un izstrādātu ārstēšanas plānu.

Nodala muskuļos neinvazīvu un muskuļos invazīvu urīnpūšļa vēzi. Muskuļos neinvazīvs urīnpūšļa vēzis ir virspusējs, agrīnas stadijas vēzis, kad vēža šūnas atrodas tikai urīnpūšļa gļotādā un nav izplatījušās dziļāk muskuļu slānī. Iedala zema riska, vidēja riska, augsta riska un ļoti augsta riska muskuļos neinvazīvu urīnpūšļa vēzi. Savukārt muskuļos invazīvs urīnpūšļa vēzis ir tāds audzējs, kas izplatījies par gļotādu dziļākos urīnpūšļa slāņos.
Urīnpūšļa vēža TNM klasifikācija un klīniskās stadijas
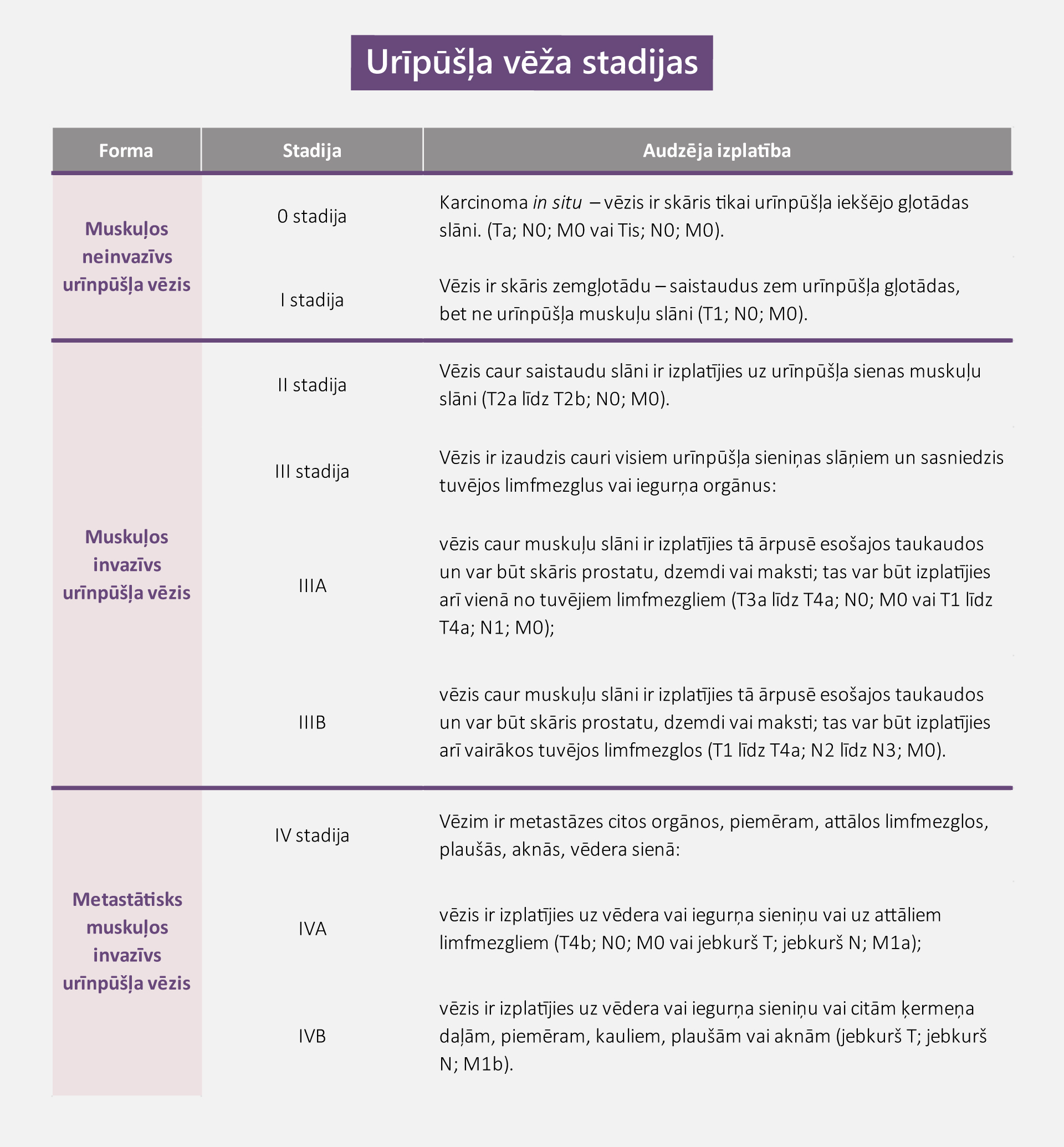
Urīnpūšļa vēža stadijas tiek klasificētas pēc TNM stadiju noteikšanas sistēmas. Šajā klasifikācijas sistēmā ar T tiek aprakstīts, cik tālu audzējs ir ieaudzis urīnpūšļa sienā, N raksturo to, vai vēzis ir izplatījies tuvējos limfmezglos, savukārt M – vai vēzim ir metastāzes citos orgānos. Vienlaikus onkoloģijā lieto arī klīnisko stadiju klasifikāciju – apvienojot atsevišķos TNM rādītājus kopējās stadijās (0–IV), iespējams sistemātiski raksturot slimības apjomu un saistīt slimības izplatību ar prognozi.19 20
Dati rāda, ka sievietēm urīnpūšļa vēzis tiek atklāts vēlīnākās stadijās nekā vīriešiem, visticamāk, tādēļ, ka sievietēm šī vēža simptomi tiek maldīgi noturēti par urīnceļu infekcijas izpausmēm.21
Audzēja diferenciācijas (ļaundabīguma) pakāpe
Papildus T, N un M rādītājiem, kas raksturo, cik tālu vēzis ir izplatījies organismā, ārsti novērtē arī audzēja diferenciācijas pakāpi jeb ļaundabīguma pakāpi (angliski – grade). Tā parāda, kā vēža šūnas izskatās mikroskopā salīdzinājumā ar normālām urīnpūšļa šūnām.
| Pakāpe | Ko tas nozīmē pacientam? |
|---|---|
| Zemas pakāpes (low-grade) | Šūnas ir līdzīgākas normālām šūnām. Audzējs parasti aug lēnāk un ir mazāk agresīvs. |
| Augstas pakāpes (high-grade) | Šūnas ļoti atšķiras no normālām. Audzējs mēdz augt straujāk un ir lielāka iespēja, ka tas izplatīsies dziļāk urīnpūslī vai citos orgānos. |

Urīnpūšļa vēža dzīvildzes rādītājs (cilvēku īpatsvars, kas ir dzīvi noteiktu laika periodu – piemēram, piecus gadus – pēc diagnozes noteikšanas) ir atkarīgs no dažādiem faktoriem, piemēram, no vēža izplatības un paveida, pacienta vecuma, vispārējā veselības stāvokļa un no tā, vai vēzis ir diagnosticēts agrīni vai arī ir recidivējis jeb atjaunojies.

Tas ir statistisks rādītājs, kas tiek aprēķināts, balstoties uz lielām cilvēku grupām, un to nevar izmantot, lai precīzi prognozētu, kas notiks ar katru atsevišķu saslimušo. Šī statistika balstās datos par daudziem tūkstošiem cilvēku ar konkrēto diagnozi, tādēļ sniedz tikai vispārīgu priekšstatu par dzīvi ar šo vēzi, taču tā nav konkrēta prognoze katram individuālajam slimības gadījumam. Piemēram, paredzamais dzīves garums var būt lielāks nekā vidējie statistiskie rādītāji, ja cilvēkam nav citu saslimšanu un kopējais veselības stāvoklis ir labs.
Turklāt jāņem vērā, ka dzīvildzes statistikā iekļauti cilvēki, kuru diagnoze uzstādīta ne mazāk kā pirms pieciem gadiem, tātad paši jaunākie medicīnas sasniegumi un jaunas ārstēšanas iespējas šajā statistikā neatspoguļojas.Ja urīnpūšļa vēzis atklāts stadijā, kad tas vēl nav skāris urīnpūšļa muskuļu slāni, ārstēšana parasti ir daudz veiksmīgāka un dzīvildzes prognoze laba.
Dzīvildze atkarībā no slimības izplatības
Dzīvildzes rādītāji parāda, cik procenti pacientu dzīvo vismaz 5 gadus pēc diagnozes noteikšanas. Tie ir statistiski dati un nevar precīzi paredzēt katra cilvēka individuālo situāciju.Balstoties uz slimības izplatību, aptuvenie 5 gadu dzīvildzes rādītāji ir šādi:22
| I stadija | 80% |
| II stadija | 45% |
| III stadija | 40% |
| IV stadija | 10% |

Ārstēšana ir atkarīga no audzēja lieluma un stadijas, kā arī no vispārējā veselības stāvokļa. Pirms tiek pieņemts lēmums par piemērotāko ārstēšanu, tiek veikti visi nepieciešamie radioloģiskie un laboratoriskie izmeklējumi, kam seko multidisciplinārs ārstu konsīlijs. Konsīlijā piedalās dažādi ar vēža ārstēšanu saistīti speciālisti, piemēram, radiologi, onkologs ķīmijterapeits, urologs, staru terapeits, patologs; pēc nepieciešamības tiek piesaistīti arī citi eksperti.

Publiski pieejami vairāki drošticami informatīvie resursi par urīnpūšļa vēzi. Rokasgrāmatas un vadlīnijas izdevusi gan Eiropas Urologu asociācija (European Association of Urology, EAU), gan Eiropas Onkologu ķīmijterapeitu biedrība (European Society For Medical Oncology, ESMO), kā arī ASV Nacionālais visaptverošais vēža tīkls (National Comprehensive Cancer Network, NCCN).
Vēža ārstēšanas veidus iedala lokālajos un sistēmiskajos. Sistēmiskā terapija ir ārstēšanas veids, kad medikamentu ievada asinsritē, un tas sasniedz visas ķermeņa daļas. Pie sistēmiskās terapijas pieder ķīmijterapija, imūnterapija un mērķterapija (citu vēžu gadījumā – arī hormonterapija). Savukārt ķirurģija un staru terapija ir lokālas ārstēšanas metodes. Sistēmiskās un lokālās terapijas metodes var kombinēt.
Lielākajā daļā gadījumu urīnpūšļa vēža ārstēšana ietver vairākas terapijas metodes. To izvēle un secība atšķiras katrā konkrētajā gadījumā: reizēm pirms ķirurģijas var būt nepieciešama ķīmijterapija, kas samazinātu audzēja izmēru; ir gadījumi, kad pirms un pēc ķirurģijas nozīmē imūnterapiju; dažreiz vienīgā ārstēšanas pieeja ir ķīmijterapija.
Ja audzējs nav plaši izplatījies, tad ārstēšanu parasti sāk ar operāciju – transuretrālu urīnpūsļa rezekciju. Operācijas mērķis ir ne tikai ārstēt, bet arī diagnosticēt, jo izoperētais materiāls tiek nosūtīts patohistoloģiskai izmeklēšanai, lai ārsts patologs, izanalizējot vēža šūnas, noteiktu audzēja tipu un agresivitātes pakāpi. Patologa slēdziens ir viens no svarīgākajiem posmiem vēža diagnozes noteikšanā un būtiski ietekmē tālāko ārstēšanas taktiku un slimības prognozi. Atkarībā no audzēja stadijas, ārstu konsīlijs lemj par tālāko ārstēšanas gaitu. Ja tiek diagnosticēts plašs vai agresīva tipa vēzis, pēc operācijas tiek nozīmēta adjuvanta ķīmijterapija vai imūnterapija. Tā ir terapija, ko piemēro pēc pamata (primārās) ķirurģiskas ārstēšanas, lai atbrīvotos no vēža šūnām, kas var būt palikušas pāri pēc operācijas.
Gadījumos, kad audzējs ir plaši izplatījies un sākotnēji nav iespējams veikt radikālu ķirurģisku ārstēšanu, ārstēšanu sāk ar neoadjuvanto jeb pirmsoperācijas ķīmijterapiju – tādā veidā tiek samazināts audzēja izmērs, lai vēlāk, ja iespējams, veiktu operāciju.
Ķirurģiskās ārstēšanas mērķis ir izņemt audzēju un dažkārt arī apkārtējos audus. Ķirurģiskas procedūras var būt dažādas – sākot ar neliela veidojuma atdalīšanu no urīnpūšļa gļotādas līdz pat pilnīgai urīnpūšļa un citu orgānu izņemšanai.
Urīnpūšļa vēža ķirurģiskas ārstēšanas metodes:
Ja operācijas laikā urīnpūslis tiek izņemts, tiek izveidots jauns urīna atteces ceļš:
Izmaiņas urinēšanā ir būtiska cistektomijas blakusparādība un var ilgtermiņā ietekmēt pacienta fizisko un emocionālo labsajūtu.
Kā jau pēc jebkuras operācijas, arī pēc urīnpūšļa vēža operācijas pastāv komplikāciju risks – komplikācijas piedzīvo aptuveni trešā daļa pacientu. Daudzas komplikācijas ir vieglas, bet dažas var būt dzīvībai bīstamas.
Pēc cistektomijas iespējami šādi sarežģījumi:
Lai veicinātu atveseļošanos un mazinātu komplikāciju risku, vēlams pēc iespējas ātrāk atsākt kustēties un nodarboties ar fiziskām aktivitātēm.
Ķīmijterapija ir viena no vēža ārstēšanas metodēm, kurā izmanto medikamentus, kas iznīcina vēža šūnas, kavējot to augšanu vai vairošanos. Urīnpūšļa vēža ārstēšanā ķīmijterapiju izmanto gan agrīnās, gan progresējušās stadijās.
Ķīmijterapiju nozīmē atkārtotu kursu veidā – viens kurss ietver periodu, kad tiek saņemta terapija (piemēram, noteikts dienu skaits ar medikamenta ievadi vienreiz dienā), kā arī atpūtas periodu, kuru pacients parasti pavada mājās. Šādu kursi atkārto vairākas reizes, piemēram, 2-3 mēnešu laikā var būt 3-6 ķīmijterapijas kursi. Ārstēšanas shēma un zāļu veids ir atkarīgs no audzēja stadijas un veida, pacienta vispārējā veselības stāvokļa un blakusslimībām.
Urīnpūšļa vēža gadījumā tiek izmantoti divi galvenie ķīmijterapijas ievadīšanas veidi:
Ķīmijterapijas medikamenti iedarbojas ne tikai uz vēža šūnām, bet arī uz veselajām šūnām, kurām raksturīga ātra dalīšanās, piemēram, matu folikulos un šūnas, kas izklāj gremošanas traktu. Blakusparādības ir ļoti individuālas un atkarīgas no zāļu veida un devas. Vairums no tām ir īslaicīgas un kontrolējamas.
Vairums pacientu jūtas noguruši, samazinās apetīte, izraisot svara zudumu, var būt slikta dūša vai vemšana, iespējama caureja.
Bieži ķīmijterapija izraisa noteikta veida asinsķermenīšu skaita samazināšanos:
Asinsaina ķīmijterapijas laikā tiek regulāri uzraudzīta, lai nepieciešamības gadījumā ārstēšanu mainītu.
Kā sagatavoties ķīmijterapijai lasiet: ŠEIT.
Virspusēja urīnpūšļa vēža ārstēšanai lieto arī terapiju ar Kalmeta-Gerēna baktēriju (Bacillus Calmette-Guérin, BCG). Urīnpūslī ievada šķīdumu ar dzīvu, bet novājinātu Mycobacterium bovis baktēriju, kas ierosina spēcīgu imūnsistēmas atbildes reakciju, liekot tai iznīcināt vēža šūnas. Šī terapija samazina audzēja atkārtošanās un progresēšanas risku un tiek izmantota gadījumos, kad vēzis nav cauraudzis urīnpūšļa muskuļu sāni. Ārstēšanu parasti uzsāk 3–6 nedēļas pēc TURBT, preparātu ievada vienu reizi nedēļā un ārstēšanas kurss ilgst sešas nedēļas. Atkarībā no vēža atkārtošanās riska terapiju var turpināt kā uzturošo ārstēšanu vairākus gadus.
Iespējamās intravezikālās BCG terapijas blakusparādības ir drudzis, drebuļi, pēkšņa vajadzība urinēt, sāpes vai diskomforts urinēšanas laikā, kā arī asinis vai asins recekļi urīnā.
Intravezikālā terapija ir ārstēšana, kad zāles ievada tieši urīnpūslī caur katetru (visbiežāk pēc virspusēja urīnpūšļa audzēja izņemšanas), lai iedarbotos lokāli uz gļotādu un samazinātu recidīva risku. Tā kā zāles pārsvarā darbojas urīnpūslī, blaknes visbiežāk ir lokālas.
Staru terapija ir augstas enerģijas starojuma (rentgena stari, gamma stari, neitroni, protoni un citi) izmantošana vēža šūnu iznīcināšanai un audzēju samazināšanai. Ārstējot urīnpūšļa vēzi, staru terapiju visbiežāk izmanto vienu pašu vai kopā ar ķīmijterapiju.
Visbiežāk izmanto ārējo jeb distances staru terapiju, kad starojums tiek raidīts no iekārtas ārpus ķermeņa. Šī procedūra ir īsa un nesāpīga. Pirms staru terapijas uzsākšanas pacientam tiek veikta ārstēšanas kursa plānošana: veikts datortomogrāfijas vai rentgena izmeklējums un uz pacienta ādas veiktas speciālas atzīmes, kas pirms katra staru terapijas seansa palīdz precīzi pozicionēt apstarojamās ķermeņa vietas. Var tikt izgatavota arī speciāla veidne, kas palīdz augumu noturēt nekustīgā stāvoklī. Plānošanas sesija var ilgt līdz 2 stundām. Staru terapijas seansi parasti notiek 5 reizes nedēļā, un viss ārstēšanas kurss var ilgt no dažām dienām līdz vairākām nedēļām.
Retāk novēro tādas ilgtermiņa blakusparādības kā urīnpūšļa izmēra samazināšanās (var izraisīt ļoti biežu nepieciešamību urinēt) vai zarnu bojājumus (var izpausties kā caureja un grūtības kontrolēt vēdera izeju). Šīs blakusparādības ir retas, taču par jebkādiem simptomiem noteikti jāinformē ārstējošais personāls, kas ieteiks, kā mazināt simptomus.
Trimodāla terapija ir ārstēšanas pieeja, kas apvieno trīs metodes. Šīs pieejas mērķis ir izārstēt slimību un vienlaikus saglabāt urīnpūsli. Vispirms tiek veikta transuretrāla rezekcija, audzēju izņemot caur urīnizvadkanālu (TURB operācija), pēc tam seko staru terapija, kas iznīcina atlikušās vēža šūnas, un ķīmijterapija mazās devās, lai pastiprinātu staru terapijas efektu. Šī pieeja ir piemērota, piemēram, muskuļslānī ieauguša urīnpūšļa vēža gadījumā, jo tā parasti ir iespējams panākt labu audzēja kontroli bez visa urīnpūšļa izņemšanas.
Imūnterapija palīdz stiprināt vai atjaunot imūnsistēmas spēju cīnīties ar vēzi, iznīcināt audzēja šūnas un apturēt to augšanu un izplatīšanos. Agrīnā stadijā, kad audzējs nav iespiedies urīnpūšļa muskuļu slānī, imūnterapijas medikamentu ievada tieši urīnpūslī jeb intravezikāli. Šāda metode ir, piemēram, imūnterapija ar Bacillus Calmette-Guerin (BCG) – ievadot urīnpūslī novājinātu tuberkulozes baktēriju, tiek izraisīta spēcīga imūnā reakcija pret vēža šūnām.
Metastātiska urīnpūšļa vēža gadījumā parasti lieto imūnsistēmas kontrolpunktu inhibitoru terapiju. Svarīga imūnsistēmas funkcija ir tās spēja neuzbrukt normālām organisma šūnām. Tas iespējams, pateicoties "kontrolpunktiem" – olbaltumvielām uz imūnšūnām, kuras tiek aktivizētas, lai sāktos imūnā reakcija. Vēža šūnas izmanto šos kontrolpunktus, lai izvairītos no imūnsistēmas uzbrukuma. Medikamentus, kas iedarbojas uz šiem kontrolpunktiem, sauc par imūnsistēmas kontrolpunktu inhibitoriem, un tie ļauj imūnsistēmas šūnai “pamanīt” vēža šūnu un to iznīcināt.27
Viena no kontrolpunktu inhibitoru grupām ir PD-1 un PD-L1 inhibitori. PD-1 un PD-L1 ir kontrolpunkti uz imūnsistēmas T šūnām, kuru funkcija ir neļaut T šūnām uzbrukt citām organisma šūnām. Pie PD-1 un PD-L1 kontrolpunktu inhibitoru grupas pieder, piemēram, intravenozi ievadāmi imūnterapijas medikamenti pembrolizumabs, atezolizumabs, avelumabs, nivolumabs, durvalumabs.28 29
Lai izvērtētu, vai pacientam ar progresējošu vai metastātisku urīnpūšļa vēzi ir piemērota ārstēšana ar imūnsistēmas kontrolpunktu inhibitoriem, tiek noteikta PD-L1 receptoru ekspresija (klātbūtne un daudzums) audzēja šūnās. Šis rādītājs palīdz prognozēt iespējamo terapijas efektivitāti un pieņemt pamatotu lēmumu par ārstēšanas izvēli.
Imūnsistēmas kontrolpunktu inhibitoru terapijas blakusparādības rodas tādēļ, ka pastiprināti aktivētā imūnsistēma var sākt uzbrukt arī organisma veselajiem audiem, izraisot tā sauktās imūnmediētās reakcijas. Blakņu smaguma pakāpe var būt ļoti dažāda – no vieglām un pārejošām līdz nopietnām vai pat dzīvībai bīstamām. Tās var atšķirties arī atkarībā no konkrētā imūnterapijas medikamenta.
Tomēr vairums blakusparādību ir veiksmīgi kontrolējamas, ja tās tiek savlaicīgi atpazītas un ārstētas. Smagu vai nekontrolējamu blakņu gadījumā ārstēšanu ar konkrēto imūnterapijas līdzekli nepieciešams pārtraukt un uzsākt atbilstošu terapiju blakusparādību mazināšanai.
Blaknes visbiežāk ietekmē šo ķermeņa daļu darbību:30
Bez minētajām blaknēm bieži novēro arī plaukstu-pēdu sindromu, elpas trūkums jeb dispnoja, paaugstināts asinsspiediens, nogurumu un sliktu dūšu, galvassāpes, urīnceļu problēmas, anēmiju, locītavu sāpes jeb artralģiju, tūsku.
Mērķterapijā tiek izmantotas zāles, kas selektīvi iedarbojas uz konkrētām molekulām (piemēram, olbaltumvielām vai receptoriem) uz vēža šūnu virsmas vai to iekšienē. Šīs molekulas piedalās signālu pārraidē, kas veicina audzēja šūnu augšanu, dalīšanos un izdzīvošanu. Precīzi bloķējot vai kavējot šo signālu darbību, iespējams palēnināt vai apturēt vēža šūnu augšanu un izplatīšanos, vienlaikus mazāk ietekmējot veselās šūnas nekā tradicionālā ķīmijterapija.
Mērķterapiju lieto galvenokārt cilvēkiem ar specifiskām gēnu mutācijām – šīs mutācijas ir mērķterapijas medikamentu “mērķis”. Pacientiem bez gēnu mutācijām mērķterapija nav piemērota.31
Urīnpūšļa vēža ārstēšanai var izmantot vairākas mērķterapijas pieejas:
Tas, kādas un cik izteiktas blakusparādības būs, lietojot mērķterapijas medikamentus, atkarīgs no dažādiem faktoriem – pacienta vispārējā veselības stāvokļa, konkrētā medikamenta un tā, vai tiek lietotas vienas vai vairākas zāles, kā arī no medikamenta devas. Lielāko daļu blakņu var veiksmīgi kontrolēt ar medikamentu vai dzīvesveida izmaiņu palīdzību.
Enfortumaba-vedotīna blakusparādības:
Novēro arī acu kairinājumu un sausās acs sindromu un disgeiziju jeb garšas izjūtas izmaiņas.
Erdafitiniba blakusparādības:
Simptomātiskā terapija ir vēža simptomu un dažādu terapijas blakusparādību ārstēšana, visbiežāk – paliatīvās aprūpes ietvaros, kad citas ārstēšanas iespējas ir izsmeltas. Regulāras cistoskopijas, kuras veic, lai pārbaudītu, vai vēzis nav atgriezies, var izraisīt urīnpūšļa kairinājumu (piemēram, sāpes urinēšanas laikā vai bieža urinēšana) un urīnceļu infekcijas. Par šīm un līdzīgām parādībām jāinformē ārstējošais personāls, kas palīdzēs tikt ar tām galā un, ja nepieciešams, nozīmēs medikamentus.
Ja iepriekš veikta radikāla cistektomija, pacientam būs jāpielāgojas izmaiņām urinācijā un urīna novadīšanas veidā. Tas var nozīmēt stomas aprūpes prasmju apgūšanu (ja izveidota urostoma) vai pielāgošanos jaunizveidotam urīnpūšļa aizvietojumam. Atsevišķos gadījumos nozīmīgi ir arī iegurņa pamatnes un vēdera muskulatūras vingrinājumi, kas palīdz uzlabot urīna aizturi un izvadīšanas kontroli, kā arī veicina labāku dzīves kvalitāti.
Būtiska vēža ārstēšanas sastāvdaļa ir rehabilitācija. Tās mērķis ir sekmēt, lai cilvēks vēža ārstēšanas laikā un pēc tās varētu atgriezties ierastajā dzīvē un veikt ikdienas aktivitātes. Rehabilitācijas pakalpojumus sniedz multidiscpilināra speciālistu komanda, kurā parasti ietilpst psihologs, fizioterapeits, ergoterapeits, uztura speciālists, onkoloģiskās aprūpes māsa, arī mākslas vai mūzikas terapeits un sociālais darbinieks. Fizioterapija palīdz mazināt sāpes, stīvumu, nejutīgumu, kustību ierobežojumus vai citas fiziskās problēmas, kas radušās ārstēšanas rezultātā, savukārt ergoterapija palīdz atgūt spēju veikt ikdienas uzdevumus, sākot ar ģērbšanos vai ēst gatavošanu un beidzot ar atgriešanos darbā.
Ar vēža ārstēšanu saistītā noguruma, trauksmes, stresa, depresijas, bezpalīdzības pārvarēšanā atbalstu sniedz psihologs. Rehabilitācijas plāns tiek piemērots katram pacientam individuāli, atkarībā no funkcionēšanas traucējumu pakāpes. Vieglu vai mērenu funkcionēšanas grūtību gadījumā rehabilitācija parasti notiek ambulatori, smagāku funkcionēšanas traucējumu gadījumā rehabilitāciju nodrošina stacionārā.
Lasīt vairāk>> Saite uz sadaļu “Rehabilitācija”
Pēc tam, kad vēža ārstēšana ir pabeigta, pacients turpina atrasties onkologa uzraudzībā turpmākos piecus gadus. Šajā laikā būs regulāri jāveic izmeklējumi, piemēram, urīna un asins analīzes, cistoskopija, datortomogrāfija, kā arī jāapmeklē ārsts. Vēža ārstēšana var izraisīt ilgtermiņa blakusparādības (tās, kas rodas ārstēšanas laikā vai īsi pēc tās un ilgst mēnešus vai gadus) un vēlākas blakusparādības (blakusparādības, kas rodas mēnešus vai gadus pēc slimības diagnosticēšanas vai ārstēšanas beigām).
Tomēr blakusparādības parasti var kontrolēt gan ar medikamentiem, gan citām pieejām. Regulāri tiks veikta kaulu blīvuma pārbaude, lai novērstu osteopēnijas un osteoporozes risku. Kaulu blīvuma samazināšanās ārstēšanai var būt nepieciešami medikamentus. Vēlams regulāri veikt D vitamīna līmeņa analīzes. Vienmēr nekavējoties jāziņo ārstam, ja parādās nebijuši simptomi vai ja pastiprinās līdzšinējie.
Vairāk par D vitamīnu lasiet: ŠEIT.

Nav viena droša un pierādīta veida, kā novērst urīnpūšļa vēzi. Dažus riska faktorus, piemēram, līdzšinējo saslimšanu vēsturi vai iedzimtību, nav iespējams ietekmēt. Tādēļ profilakses pasākumi vērsti galvenokārt uz dzīvesveida izmaiņām, apkārtējo vidi un saskari ar kancerogēnām vielām.

Lai samazinātu iespēju saslimt ar urīnpūšļa vēzi, ieteicams:
