


Kuņģa vēzis ir viens no biežāk sastopamajiem audzējiem – tas ir piektais visbiežāk diagnosticētais vēzis pasaulē. Vairāk nekā 90% gadījumu šis audzējs ir adenocarcinoma, kas sākas kuņģa gļotādā. Kuņģa vēža attīstība visbiežāk saistīta ar Helicobacter pylori infekciju, neveselīgu uzturu, smēķēšanu un ģenētiskiem faktoriem. Sākotnējās stadijās kuņģa vēža simptomi ir vāji izteikti vai viegli sajaucami ar gremošanas traucējumiem. Ārstēšana ir atkarīga no stadijas un veida, bet visbiežāk ir nepieciešama ķirurģiska operācija un ķīmijterapija, arī staru terapija, retāk izmanto mērķterapiju vai imūnterapiju. Tā kā sākotnējie simptomi ir vāji izteikti, daudziem pacientiem diagnoze tiek noteikta vēlīnā stadijā, tāpēc svarīgi laikus vērsties pie ārsta, ja parādās aizdomīgi, nepārejoši simptomi.

Kuņģis – liels, dobs muskuļu orgāns – ir daļa no gremošanas sistēmas. Tas izdala gremošanas sulas un skābi, kas palīdz sašķelt uzņemto pārtiku un pārvieto to tālāku uz tievajām zarnām, kur pārtika tiek sagremota un absorbēta. Sieniņa, kas ieskauj šo gremošanas orgānu, sastāv no daudziem slāņiem – tieši tajos sāk veidoties kuņģa vēzis. Šis audzējs attīstās, kad ģenētiski bojātas kuņģa gļotādas šūnas sāk vairoties un nekontrolēti augt. Audzējs veidojas kuņģa sienas iekšējā slānī un aug cauri šīs sienas slāņiem.
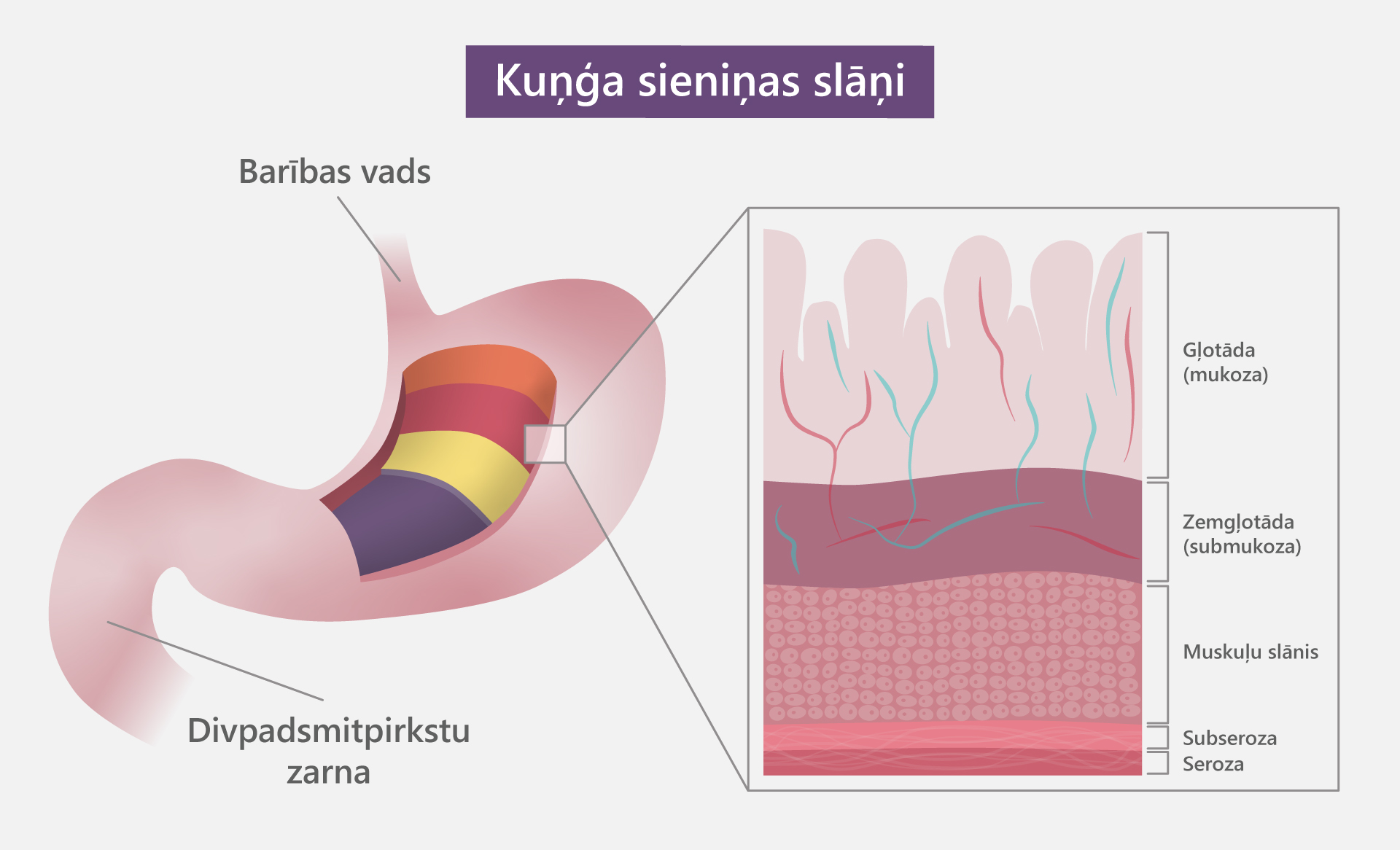
Kuņģim ir pieci slāņi:
• iekšējais slānis (mukoza) – gļotāda, kas izdala kuņģa skābi un citus gremošanas fermentus; te visbiežāk sāk veidoties vēzis;
• zemgļotāda (submukoza);
• muskuļu slānis – sastāv no muskuļiem, kas kustoties sajauc kuņģa saturu;
• subseroza – audu slānis starp serozu un kuņģa muskuļoto slāni. Serozas un subserozas funkcija ir aizsargāt kuņģi, samazinot berzi, kas rodas iekšējiem orgāniem kustoties.
• seroza – plāns saistaudu slānis, kas klāj kuņģi no ārpuses;
Kuņģa vēzis ir piektais izplatītākais vēža veids pasaulē. Latvijā ik gadu to diagnosticē ~ 600 cilvēkiem, savukārt ~500 pacientu kuņģa vēža dēļ mirst. Šis audzējs biežāk sastopams gados vecākiem cilvēkiem – aptuveni puse gadījumu konstatēta pacientiem, kas vecāki par 75 gadiem. Tas divkārt biežāk skar vīriešus nekā sievietes.
Kuņģa vēzi var iedalīt paveidos pēc tā, kurā kuņģa daļā audzējs rodas – tas var notikt jebkurā kuņģa daļā, taču visbiežāk tā attīstība sākas kuņģa iekšējās gļotādas dziedzeru šūnās, un šo vēža veidu sauc par adenokarcinomu. Retāk sastop plakanšūnu karcinomu, kas attīstās no plakanajām šūnām, kuras klāj kuņģa virsmu, kā arī kuņģa-zarnu trakta stromas audzēju, kas ir reta sarkomas forma. Tomēr aptuveni 90% no visiem kuņģa vēža gadījumiem ir tieši adenokarcinomas.

Nereti kuņģa vēzim nav īpaši izteiktu pazīmju, it sevišķi tā agrīnajās stadijās.

Pazīmes var būt grūti pamanāmas vai līdzināties vispārējiem gremošanas traucējumiem.
Izplatītākās kuņģa vēža izpausmes ir šādas:
Šie simptomi var parādīties arī citu veselības traucējumu gadījumā un nenozīmē, ka kuņģī noteikti attīstās audzējs. Tomēr, saskaroties ar jebkuru no šiem simptomiem, jāgriežas pie ārsta.

Riska faktori ir personīgi, dzīvesveida, vides vai iedzimtības aspekti, kas palielina iespēju saslimt ar kādu slimību, šajā gadījumā kuņģa vēzi.


Tiek aktīvi pētītas kuņģa vēža skrīninga iespējas, kas ļautu atklāt šo audzēju agrīnās stadijās, kad izredzes to izārstēt ir vislielākās. Tomēr pagaidām kuņģa vēzim Eiropā nav izstrādātas vienotas skrīninga programmas. Šī iemesla dēļ, kā arī vāji izteikto agrīno pazīmju vai pat to trūkuma dēļ kuņģa vēzis bieži tiek atklāts salīdzinoši vēlīnā stadijā.

Pastāvot aizdomām par kuņģa vēzi, ārsts vispirms iztaustīs vēderu, lai konstatētu iespējamu pietūkumu, sāpes vai citu netipisku parādību. Tiks izklausīts ne vien vēdera dobums, bet arī krūškurvis (plaušas un sirds).
Ārsts var pārbaudīt:
• ķermeņa temperatūru, asinsspiedienu, pulsu un elpošanu
• svaru un auguma garumu
• acis, ausis, degunu un rīkli
• limfmezglus kaklā, padusēs un cirkšņos
Tiks novērtēts cilvēka vispārējais fiziskais stāvoklis, kas palīdz izlemt par piemērotāko ārstēšanu, ja tāda būs nepieciešama. Bez klīniskajiem izmeklējumiem nepieciešams veikt arī fēču analīzes.
Helicobacter pylori (H. pylori) ir baktērija, kas izraisa kuņģa gļotādas infekciju. Tā palielina risku saslimt ar kuņģa vēzi. Testu helikobaktērijas noteikšanai var veikt, gan izmantojot asins analīzes, gan elptestu, gan nododot izkārnījumu (fēču) paraugu. Ja cilvēkam tiek atklāta šīs baktērijas infekcija, tā jāārstē, un H. pylori testu vēlams veikt arī citiem ģimenes locekļiem. Pastāvot aizdomām par kuņģa vēzi, ārsts vispirms iztaustīs vēderu, lai konstatētu iespējamu pietūkumu, sāpes vai citu netipisku parādību. Tiks izklausīts ne vien vēdera dobums, bet arī krūškurvis (plaušas un sirds).
Biopsija ir procedūra, kuras laikā no orgāniem tiek paņemts audu paraugs, ko nosūta pārbaudei laboratorijā, lai noteiktu slimības klātbūtni. Vēža gadījumā biopsiju parasti veic endoskopijas laikā, reizēm var būt nepieciešams paņemt vairākus paraugus – ne tikai no kuņģa, bet arī no barības vada, limfmezgliem vai orgāniem netālu no kuņģa, piemēram, aknām.
Citi biopsijas veidi:
- Aspirācijas biopsija un “core” biopsija – audu paraugu paņemšanai tiek izmantota adata. Precīzākai procedūras norisei ārsts biopsiju var veikt ultrasonogrāfijas kontrolē.
- Audzēja šūnu paraugu var paņemt arī ar nelielu otai līdzīgu instrumentu, kas piestiprināts endoskopam (brush biopsy).
- Skalojumi – izmantojot sterilu šķidrumu, tiek skalots vēdera dobums. Šķidrums pēc tam tiek pārbaudīts, lai konstatētu, vai tajā nav vēža šūnu. Skalojumus parasti veic ķirurģiskas operācijas laikā.
- Šķidrā biopsija – testēšanai tiek izmantots asins paraugs.
Biomarķieri ir bioloģiskas molekulas, kas var liecināt par vēža klātbūtni organismā. Tās ražo vai nu pats audzējs, vai organisma veselās šūnas, reaģējot uz audzēju. Biomarķieru testi, tāpat kā visi pārējie izmeklējumi, palīdz izvēlēties vispiemērotāko ārstēšanas veidu un taktiku. Vienlaikus jāatceras, ka biomarķieru līmeni var ietekmēt arī ar audzēju nesaistīti procesi.
Audzēja mutāciju testēšana ir diagnostikas pieeja, kuras mērķis, izmantojot audzēja audu paraugu vai asins paraugu, ir pārbaudīt, vai vēža šūnās ir kādas specifiskas DNS mutācijas. Atšķirībā no ģenētiskajiem testiem, kas nosaka no vecākiem pārmantotas ģenētiskās mutācijas, audzēja mutāciju testēšanas laikā meklē ģenētiskas izmaiņas pašā ļaundabīgajā veidojumā. Tas ļauj izvēlēties tādu ārstēšanu, kas vislabāk iedarbojas uz konkrēto mutāciju. Audzēja mutāciju testu visbiežāk veic tad, ja vēzis nav operējams vai ir metastātisks. Specifiskas audzēja mutācijas, kurām pastāv efektīvas terapijas, ir, piemēram, NTRK gēna saplūšana, RET gēna saplūšana vai BRAF V600E mutācija.
Visbiežāk viens no pirmajiem izmeklējumiem, kad pastāv aizdomas par kuņģa vēzi. Tās laikā ķermenī tiek ievadīta (visbiežāk caur muti) plāna, elastīga caurulīte, kurai piestiprināta kamera. Projicējot attēlu uz ekrāna, iespējams apskatīt barības vada, kuņģa un divpadsmitpirkstu zarnas iekšpusi. Endoskopijas laikā ārsts var veikt biopsiju – paņemt audu paraugus no orgāna vietas, kas izskatās netipiski, lai tos varētu nodot pārbaudei laboratorijā. Parasti tiek lietoti īpaši medikamenti – sedatīvi, kas pacientam izmeklējuma laikā palīdz atslābināties.

Vēža stadija un pakāpe atspoguļo to, cik tālu un cik ātri vēzis ir izplatījies. Šī informācija nepieciešama, lai prognozētu slimības gaitu un izstrādātu ārstēšanas plānu.

Kuņģa vēža stadijas tiek klasificētas pēc TNM stadiju noteikšanas sistēmas. Šajā klasifikācijas sistēmā ar T tiek aprakstīts, cik tālu audzējs ir ieaudzis kuņģa sienā, N raksturo to, vai vēzis ir izplatījies tuvējos limfmezglos, savukārt M – vai vēzim ir metastāzes citos orgānos. Saskaņā ar TNM klasifikācijas sistēmu, kuņģa audzējam ir piecas stadijas, kuras apzīmē ar romiešu cipariem no 0 līdz IV – jo mazāks stadiju apzīmējošais skaitlis, jo labāka ir ārstēšanas prognoze.

Kuņģa vēža stadijas precizēšanai izmanto arī molekulāros testus. Analizējot biopsijas paraugus un konstatējot specifiskas bioloģiskas molekulas (biomarķierus) vēža šūnās, iespējams izvēlēties visefektīvāko ārstēšanas metodi. Ja molekulārās analīzes atklāj augstu HER2 vai PD-L1 līmeni, pacientiem var piemērot specifisku terapiju. Individuāli pielāgotu ārstēšanu prasa arī vēzis ar augstu mikrosatelītu nestabilitāti vai audzējs ar nepietiekamas gēnu kļūdu labošanas (dMMR) pazīmēm.
Sākotnēji noteiktā vēža stadija var tikt mainīta pēc operācijas, jo tās laikā iegūtie audzēja un audu paraugi sniedz papildus informāciju par vēzi un ļauj precizēt diagnozi.
Audzēja stadija rāda, cik tālu vēzis ir izplatījies, taču tas nav vienīgais raksturlielums, ko lieto vēža diagnosticēšanai un ārstēšanas plānošanai. Lai aprakstītu, cik ļoti vēža šūnas atšķiras no normālām kuņģa šūnām, nosaka arī audzēja diferenciācijas pakāpi (“tumor grade”). Tas palīdz prognozēt, cik ātri vēzis var augt un izplatīties. Augstas diferenciācijas pakāpes audzēji parasti aug lēnāk, savukārt zemas diferenciācijas pakāpes audzēji mēdz būt agresīvāki.

Kuņģa vēža dzīvildzes rādītājs (cilvēku īpatsvars, kas ir dzīvi noteiktu laika periodu – piemēram, piecus gadus – pēc diagnozes noteikšanas) ir atkarīgs no dažādiem faktoriem, piemēram, no vēža stadijas, pacienta vecuma, vispārējā veselības stāvokļa un no tā, vai vēzis ir diagnosticēts agrīni vai arī ir recidivējis.

Tas ir statistisks rādītājs, kas tiek aprēķināts, balstoties uz lielām cilvēku grupām, un to nevar izmantot, lai precīzi prognozētu, kas notiks ar katru atsevišķu saslimušo. Šī statistika balstās datos par daudziem tūkstošiem cilvēku ar konkrēto diagnozi, tādēļ sniedz tikai vispārīgu priekšstatu par dzīvi ar šo vēzi, taču tā nav konkrēta prognoze katram individuālajam slimības gadījumam. Piemēram, paredzamais dzīves garums var būt lielāks nekā vidējie statistiskie rādītāji, ja cilvēkam nav citu saslimšanu un kopējais veselības stāvoklis ir labs. Turklāt jāņem vērā, ka dzīvildzes statistikā iekļauti cilvēki, kuru diagnoze uzstādīta ne mazāk kā pirms pieciem gadiem, tātad paši jaunākie medicīnas sasniegumi un jaunas ārstēšanas iespējas šajā statistikā neatspoguļojas.
| I stadija | 65% |
| II stadija | 35% |
| III stadija | 25% |
| IV stadija | 7% |

Ārstēšana ir atkarīga no audzēja lieluma, atrašanās vietas un stadijas, kā arī no vispārējā veselības stāvokļa. Pirms tiek pieņemts lēmums par piemērotāko ārstēšanu, tiek veikti visi nepieciešamie radioloģiskie un laboratoriskie izmeklējumi, kam seko multidisciplinārs ārstu konsīlijs. Konsīlijā piedalās dažādi ar vēža ārstēšanu saistīti speciālisti, piemēram, radiologi, onkologs ķīmijterapeits, vēdera dobuma ķirurgs; pēc nepieciešamības tiek piesaistīti arī citi eksperti.

Drošticamas kuņģa vēža ārstēšanas vadlīnijas izdevusi gan viena no Eiropas vadošajām profesionālajām organizācijām onkoloģijā (angļu valodā) – Eiropas Onkologu ķīmijterapeitu biedrība (European Society For Medical Oncology, ESMO), gan ASV Nacionālais visaptverošais vēža tīkls (National Comprehensive Cancer Network, NCCN).
ESMO kuņģa vēža ārstēšanas vadlīnijas angļu valodā lasāmas: ŠEIT>>
NCCN kuņģa vēža diagnostikas, stadijas noteikšanas un ārstēšanas vadlīnijas pacientiem angļu valodā lasāmas: ŠEIT>>
Lielākajā daļā gadījumu kuņģa vēža ārstēšana ietver vairākas terapijas metodes. Ja audzējs nav plaši izplatījies, tad ārstēšanu parasti sāk ar operāciju. Izoperētais materiāls tiek nosūtīts patohistoloģiskai izmeklēšanai – ārsts patologs analizē vēža šūnas, lai noteiktu audzēja tipu un agresivitātes pakāpi. Patologa slēdziens ir viens no svarīgākajiem posmiem vēža diagnozes noteikšanā un būtiski ietekmē tālāko ārstēšanas taktiku un slimības prognozi.
Atkarībā no audzēja stadijas, ārstu konsīlijs lemj par tālāko ārstēšanas gaitu. Ja tiek diagnosticēts plašs vai agresīva tipa vēzis, pēc radikālas operācijas tiek nozīmēta profilaktiska jeb adjuvanta ķīmijterapija. Tā ir terapija, ko piemēro pēc pamata (primārās) ķirurģiskas ārstēšanas, lai atbrīvotos no vēža šūnām, kas var būt palikušas pāri pēc operācijas.
Gadījumos, kad audzējs ir plaši izplatījies un nav iespējams veikt primāru radikālu ķirurģisku ārstēšanu, tā tiek sākta ar neoadjuvanto jeb pirmsoperācijas ķīmijterapiju – tādā veidā tiek samazināts audzēja izmērs, lai atvieglotu tālāk sekojošo ķirurģisko ārstēšanu.
Metastātiska kuņģa vēža ārstēšanas taktikā medikamentu secību mēdz iedalīt “līnijās”. Pirmās līnijas medikamenti ir tie, kurus lieto kā pirmās izvēles ārstēšanas taktiku. Nepieciešamības gadījumā tai var sekot otrās līnijas medikamenti – tos var izmantot, piemēram, ja slimība turpina progresēt pēc pirmās līnijas terapijas.

Ķirurģiskas operācijas mērķis ir izņemt audzēju kopā ar nelielu veselo audu slāni ap audzēju, lai novērstu tā atkārtotas parādīšanās risku. Tomēr ne visiem kuņģa vēža gadījumiem operācija ir piemērota: parasti ķirurģija nav ieteicama pacientiem ar metastātisku audzēju.
Lai ķirurģiski izoperētu visu audzēja masu, veic laparotomiju jeb atvērta tipa operāciju: vēdera dobumu atver ar plašu griezienu, kas var sniegties no krūšu kurvja lejasdaļas līdz pat mazajam iegurnim). Atklāta operācija var ilgt vairākas stundas vai ilgāk, un pēc tās jāuzturas stacionārā vēl vairākas dienas.
Agrīnas stadijas audzēja gadījumā iespējama arī laparoskopiska operācija, kad vairākās vietās vēdera sienā tiek izdarīti nelieli iegriezumi apmēram 1 cm garumā. Caur katru griezumu tiek ievadīti instrumenti, tostarp laparoskops jeb plāna caurulīte ar videokameru galā, kas ļauj ķermeņa iekšienes attēlu raidīt uz monitoru. Ķirurgs veic operāciju, skatoties monitora ekrānā. Ķirurģiskās operācijas veids ir atkarīgs no vēža stadijas:
Operācijas, kuras veic, lai atvieglotu simptomus un uzlabotu dzīves kvalitāti:
• Gastrojejunostomija – kuņģa caurejamības atjaunošana, ko veic, tievo zarnu savienojot ar kuņģa augšējo daļu. Šādi uzņemtā pārtika var “apiet” bojāto gremošanas trakta daļu un nokļūt tievajās zarnās. Šo operāciju var veikt gan laparoskopiski, gan laparotomiski.
• Barošanas stomas jeb gastrostomas izveidošana, lai atvieglotu pārtikas un šķidruma uzņemšanu. Stomu veido mīksta plastmasas caurulīte, un to var ievadīt vai nu kuņģī (G-tube), vai tievajā zarnā (J-tube). Šādi iespējams izvadīt gaisu un šķidrumu no gremošanas trakta, kā arī ievadīt tajā zāles, šķidrumu un barību. Barības uzņemšanu caur gastrostomas zondi dēvē par enterālo barošanu.
Kuņģa vēža pacientiem pēc audzēja operācijas jārēķinās ar noteiktām blakusparādībām, tostarp arī tādām, kas attīstās vēlu pēc operācijas un nepāriet ilgstoši:
Kā pēc jebkuras operācijas, arī pēc kuņģa vēža ķirurģiskas ārstēšanas būs nepieciešams laiks, lai atkoptos, it sevišķi, ja veikta atvērta tipa operācija.
Sāpes: aptuveni nedēļu pēc operācijas var saglabāties diskomforts operācijas apvidū, kas pakāpeniski mazinās; var būt nepieciešams lietot pretsāpju līdzekļus.
Ēšana un dzeršana: Pirmajās dienās pēc operācijas pacientam nereti šķidrumu ievada intravenozi, ar tā saukto sistēmu. Pakāpeniski atsākot dzert, vispirms iesaka dzert ūdeni un tikai pēc tam citus dzērienus.
Pēc gastrektomijas lielākā daļa pacientu saskaras ar ēšanas grūtībām. Pēc šādas operācijas pārtika pārāk ātri nonāk divpadsmitpirkstu zarnā, izraisot pēkšņu hormonu pieplūdumu un cukura līmeņa pazemināšanos asinīs. Tas var izraisīt reiboni, vājumu un sliktu dūšu. Jākonsultējas ar uztura speciālistu vai ārstu par to, kā šīs sajūtas novērst. Ēšanā jāievēro regularitāte, jāēd nelielām porcijām un jāizvairās no noteiktiem produktiem. Plašāka informācija lasāma Veselības ministrijas izstrādātajā materiālā “Uztura ieteikumi pēc gastrektomijas”.
Ja ievietota stoma, pirms došanās mājās no slimnīcas personāls iemācīs, kā to lietot un par to rūpēties. Parasti lielākā daļa pacientu pēc gastrektomijas spēj ēst un dzert normāli, tomēr jārēķinās, ka organismam var būt nepieciešams laiks, lai pielāgotos kuņģa vai tā daļas zaudēšanai.
Parasti novērojamas izmaiņas vēdera izejā, piemēram, var parādīties caureja, jo pārtika caur gremošanas sistēmu iet ātrāk nekā parasti. Lai samazinātu caurejas risku, jāizvairās no noteiktiem pārtikas produktiem – par to vislabāko padomu sniegs uztura speciālists. Var būt nepieciešami arī medikamenti pret caureju. Ja pēc vēdera izejas fēces peld, ir ļoti gaišas vai tām ir ļoti nepatīkama smarža, tas var liecināt par to, ka organisms nesagremo taukus. Šādos gadījumos var būt nepieciešams lietot gremošanas fermentus, lai palīdzētu sadalīt taukus.
Daudziem pacientiem pēc gastrektomijas ir grūti uzturēt veselīgu ķermeņa svaru – tas var būt saistīts gan ar apetītes zudumu, gan ar gremošanas sistēmas nespēju uzsūkt no uzņemtā uztura barības vielas. Jācenšas ēst tikpat daudz, cik parasti, tomēr vēlams ēst mazākas porcijas. Uztura speciālists var ieteikt arī augsta kaloriju satura dzērienus vai uztura bagātinātājus.
Pārvietošanās un fiziskā slodze: lai veicinātu atlabšanu, iesaka atsākt pārvietoties cik vien iespējams drīz pēc operācijas, tomēr vienlaikus jārēķinās ar nogurumu un reiboni.
Ķīmijterapija ir viena no t.s. sistēmiskās jeb medikamentozās terapijas pieejām. Tā ir vēža ārstēšana ar medikamentiem, kas iznīcina vēža šūnas, apturot to augšanu vai vairošanos. Šos medikamentus sauc arī par citotoksiskiem medikamentiem. Dažādi medikamenti iedarbojas uz atšķirīgām šūnas dzīves cikla fāzēm, bet to mērķis ir viens – apturēt audzēja augšanu un novērst slimības tālāku progresu. Ar ķīmiskajiem preparātiem var tikt bojātas arī veselas šūnas, īpaši tās, kas ātri dalās, tomēr šīs šūnas pēc ķīmijterapijas parasti atjaunojas. Parasti ķīmijterapiju ievada intravenozi (līdzekli ievadot vēnā), taču atsevišķi medikamenti ir arī tablešu un kapsulu formā. Ķīmijterapijas medikamenti, ko visbiežāk izmanto kuņģa vēža ārstēšanai, ir:
Ķīmijterapijas zāles var lietot gan vienas pašas, gan dažādās kombinācijās – šādas kombinācijas sauc par shēmām. Piemēram, FLOT ir 5-FU, folīnskābes, oksaliplatīna un docetaksela kombinācija. To, kurš medikaments vai medikamentu shēma ir piemērota konkrētajam pacientam, nosaka gan audzēja veids un stadija, gan arī pacienta vispārējais veselības stāvoklis un blakusslimības.
Pirms noteiktu veidu ķīmijterapijas (tostarp 5-FU un kapecitabīna) saņemšanas ārsts var nozīmēt pārbaudi, kas nosaka dihidropirimidīna dehidrogenāzes enzīma deficītu. Ja ir šī enzīma deficīts, pacients var tikt ārstēts ar mazāku ķīmijterapijas devu nekā parasti, vai arī ārsts var nolemt izmantot cita veida ķīmijterapiju.
Antivielu–zāļu konjugāti ir specifisks ķīmijterapijas veids, kur zāļu aktīvā viela ir ķīmiski savienota ar monoklonālajām antivielām. Monoklonālā antiviela spēj sasaistīties ar specifiskām olbaltumvielām vai receptoriem, kas atrodami noteiktu veidu šūnās, tostarp vēža šūnās. Nonākusi šūnas iekšienē, tā atbrīvo zāļu aktīvo vielu, kas nogalina vēža šūnu, nekaitējot citām šūnām.
Pie antivielu-zāļu konjugātu grupas pieder, piemēram, trastuzumaba derukstekāns, kas spēj savienoties ar cilvēka epidermālā augšanas faktora receptoriem 2 (HER2), kas atrodas uz noteiktu audzēja šūnu virsmas. Šo medikamentu lieto tad, ja molekulārās analīzes apliecina, ka konkrētais kuņģa vēzis ir HER2 pozitīvs.
Ķīmijterapijas blaknes atkarīgas no lietotā medikamenta veida un devas. Kombinējot vairākus ķīmijterapijas medikamentus, iespējams, ka attīstīsies vairākas blakusparādības vienlaicīgi. Savukārt, lietojot tikai vienu ķīmijterapijas preparātu, blakusparādību parasti ir mazāk. Blaknes ir pārejošas, un tās iespējams kontrolēt ar medikamentiem vai dzīvesveida izmaiņām.
Ķīmijterapijas medikamenti iedarbojas pārsvarā uz tādām šūnām, kurām raksturīga aktīva dalīšanās: kaulu smadzeņu šūnas, gremošanas trakta epitēlijšūnas, matu folikuli, mutes gļotāda u. tml. Vairums pacientu jūtas noguruši, samazinās apetīte, izraisot svara zudumu. Var būt slikta dūša vai vemšana, iespējama caureja. Daži pacienti novēro, ka mainās garšas sajūta – fermentu izmaiņas mutē var izraisīt metālisku garšu un pūslīšus vai čūliņas mutē.
Citas salīdzinoši izplatītas ķīmijterapijas blaknes ir anoreksija (vāja apetīte vai tās pilnīgs trūkums), edēma jeb tūska (šķidruma uzkrāšanās ķermeņa audos), elpas trūkums, traucēta aknu darbība, traucēta nieru darbība (tās profilaksei ieteicams dzert daudz šķidruma un izvairīties no alkohola), sirdsdarbības traucējumi, ototoksicitāte (iekšējās auss bojājumi, kas izraisa dzirdes un līdzsvara traucējumus).
Kā sagatavoties ķīmijterapijai lasiet: ŠEIT.
Mērķterapija ir ārstēšanas veids, kurā izmanto medikamentus, kas identificē un mērķēti iznīcina konkrētus vēža šūnu veidus, pēc iespējas mazāk kaitējot normālajām šūnām. Mērķterapija bloķē noteiktu enzīmu, olbaltumvielu vai citu vēža šūnu augšanā un izplatībā iesaistītu molekulu darbību. Mērķterapijas medikamenti iedarbojas uz konkrētu molekulāro mērķi – proteīnu vai receptoru, kas uz vēža šūnu virsmas sastopami lielākā daudzumā nekā veselajām šūnām. Tātad mērķterapija iedarbojas uz tādām ģenētiskām vai citādām atšķirībām, kas vēža šūnas atšķir no veselajām un ļauj tām neierobežoti augt un vairoties.
Mērķterapija var būt vērsta arī pret asinsvadu veidošanos audzējā vai iedarboties uz noteiktiem šūnu receptoriem, piemēram, izmantojot monoklonālās antivielas, kas ietekmē asinsvadu augšanas faktoru sistēmu vai HER2 receptoru. Tāpat mērķterapija var būt paredzēta audzējiem ar specifiskām gēnu izmaiņām, piemēram, NTRK, BRAF vai RET mutācijām. Konkrētas ārstēšanas izvēle vienmēr ir atkarīga no audzēja īpašībām, pacienta individuālās situācijas un terapijas pieejamības.
Mērķterapijas medikamenti iejaucas šūnu olbaltumu un receptoru darbībā, kas regulē arī asinsspiedienu, ādas stāvokli, zarnu darbību. Blaknes daudz neatšķiras no ķīmijterapijas blaknēm. Visbiežāk tās ir saistītas ar gremošanas sistēmu (slikta dūša, vemšana, caureja), kaulu smadzeņu nomākumu (neitropēnija, anēmija, trombocitopēnija), ādas problēmām (stomatīts, ādas un nagu bojājumi) un vispārīga rakstura sūdzībām (nespēks u.c.). Taču blaknes parasti var mazināt, mainot medikamenta lietošanas režīmu un devas.
Starp potenciāli bīstamām blakusparādībām minami sirdsdarbības traucējumi vai trombu veidošanās, tādēļ par jebkuru blakusparādību, kas parādās terapijas laikā, ir nekavējoties jāziņo ārstam.
Imūnterapija ir sistēmiskas terapijas veids, kurā izmanto dažādas vielas imūnsistēmas stimulēšanai vai nomākšanai, lai palīdzētu organismam pašam cīnīties ar vēzi. Daži imūnterapijas veidi ir vērsti tikai pret noteiktām imūnsistēmas šūnām, citi ietekmē imūnsistēmu kopumā. Šo terapijas veidu var izmantot gan vienu pašu, gan kopā ar citām ārstēšanas metodēm.
Svarīga imūnsistēmas funkcija ir tās spēja neuzbrukt normālām organisma šūnām. Tas iespējams, pateicoties "kontrolpunktiem" – olbaltumvielām uz imūnšūnām, kuras tiek aktivizētas, lai uzsāktu imūno reakciju. Vēža šūnas var izmantot šos kontrolpunktus, lai izvairītos no imūnsistēmas uzbrukuma. Medikamentus, kas iedarbojas uz šiem kontrolpunktiem, sauc par imūnsistēmas kontrolpunktu inhibitoriem. Bloķējot šos kontrolpunktus, tiek atjaunota imūnsistēmas spēja atpazīt un iznīcināt vēža šūnas.
Imūnterapiju galvenokārt piemēro metastātiska kuņģa vēža gadījumā, un tās piemērotība ir atkarīga no audzēja molekulārajām īpašībām. Imūnterapija var tikt apsvērta, ja audzējs ir noteiktu imūno marķieru pozitīvs vai ja tiek konstatētas specifiskas ģenētiskas izmaiņas, piemēram, augsta mikrosatelītu nestabilitāte vai traucēta gēnu kļūdu labošanas sistēma.
Konkrētas terapijas izvēle vienmēr tiek pieņemta individuāli, balstoties uz pacienta veselības stāvokli, audzēja bioloģiskajām īpašībām un terapijas pieejamību.
Visbiežāk imūnterapijas blaknes, ārstējot kuņģa vēzi, skar gremošanas sistēmu un vairogdziedzera funkciju. Pastāv risks, ka imūnterapija var izraisīt autoimunitāti – imūnās sistēma vēršanos pret savu organismu: šādos gadījumos imūnsistēma identificē normālus, veselīgus ķermeņa audus kā svešķermeņus un uzbrūk tiem.
Autoimunitāte var izraisīt iekaisumu jebkurā orgānā vai orgānu sistēmā. Dažos gadījumos tas var būt dzīvībai bīstami, tādēļ ir nekavējoties jāinformē ārstējošais personāls, ja, lietojot imūnterapijas zāles, parādās blakusparādības vai izteikti slikta pašsajūta. Biežākās ar imūnterapijas medikamentu lietošanu saistītās blakusparādības:
Plaša un detalizēta informācija par imūnterapijas blakusparādībām lasāma Eiropas Onkologu ķīmijterapeitu biedrības (European Society For Medical Oncology, ESMO) izdotajā rokasgrāmatā “Imūnterapijas blaknes: norādījumi pacientiem”, rokasgrāmata lasāma ESMO tīmekļa vietnē.
Staru terapija ir augstas enerģijas starojuma (rentgena stari, gamma stari, neitroni, protoni un citi) izmantošana vēža šūnu iznīcināšanai un audzēju samazināšanai. Starojums bojā vēža šūnu DNS un izraisa to bojāeju. Šī ārstēšanas metode ir piemērota nelieliem ļaundabīgiem veidojumiem vai nelielam ķermeņa reģionam, bet nederēs plašu ķermeņa zonu ārstēšanai. Staru terapiju lieto arī paliatīvi – lai atvieglotu audzēja radītās sāpes vai apturētu asiņošanu; tā var būt piemērota arī pēc ķirurģijas, ja ir aizdomas, ka operētajā vietā var būt palikušas ļaundabīgas šūnas. Ārstējot kuņģa vēzi, staru terapiju parasti apvieno ar ķīmijterapiju.
Staru terapiju visbiežāk nozīmē īsās ārstēšanas sesijās (procedūrās), kuras tiek veiktas mazās devās, vienu reizi dienā, vairākas dienas pēc kārtas, šādu ciklu atkārtojot vairākas nedēļas. Šī pieeja ir vissaudzīgākā iekšējiem orgāniem, bet vienlaikus nogalina audzēja šūnas apstarotajā zonā. Apstarošanas sesijas ir nesāpīgas un ilgst aptuveni 10-20 minūtes, taču zināmu laiku prasa sagatavošanās katrai apstarošanas procedūrai.
Vairāk par staru terapijas norisi iespējams uzzināt Rīgas Austrumu klīniskās universitātes slimnīcas Latvijas Onkoloģijas centra tīmekļa vietnes sadaļā “Bukleti onkoloģijas pacientiem”, e-brošūrā “Distances staru terapija”, kā arī video materiālā “Onkoloģijas pacienta ABC. Staru terapija”.
Staru terapija ir lokāla ārstēšanas metode, tādēļ blakusparādības parasti ir saistītas ar apstaroto ķermeņa zonu. Var parādīties dermatīts – ādas kairinājums, sāpes, pietūkums, lobīšanās apstarotajā krūškurvja pusē; šos simptomus var mazināt, lietojot īpašas ziedes. Līdz brīdim, kamēr āda ir sadzijusi, nav vēlams valkāt ciešu, spiedošu apģērbu (piemēram, krūšturus ar stīpiņām). Aptuveni gadu pēc terapijas jāizvairās no tiešas saules staru iedarbības uz apstaroto zonu. Piesardzība jāievēro arī peldoties, it sevišķi hlorētā ūdenī.
Staru terapija nereti izraisa arī sliktu dūšu, vemšanu un apetītes zudumu. Blakusparādības parasti sākas dažas dienas pēc staru terapijas sākšanas un sāk mazināties 1–2 nedēļas pēc ārstēšanas beigām.
Vairāk lasi sadaļas "Staru terapija" apakšsadaļā "Blakusparādības".
Simptomātiskā terapija ir vēža simptomu un dažādu terapijas blakusparādību ārstēšana. Kuņģa vēža ķirurģiska operācija nereti izraisa ēšanas traucējumus, tādēļ nepieciešams konsultēties ar uztura speciālistu par to, kā un ko ēst pēc operācijas, lai nodrošinātu pietiekamu uzturvielu nodrošinājumu un saglabātu veselīgu svaru. Kuņģa vai tā daļas izņemšana var ietekmēt vitamīnu un minerālvielu uzsūkšanos tādēļ bieži papildus jālieto kalcijs, D vitamīns, dzelzs vai B12 vitamīns.
Ja audzējs bloķē ieeju kuņģī vai divpadsmitpirkstu zarnā, izmanto stentu, kas ļauj uzņemtajai pārtikai brīvi pārvietoties gremošanas traktā. Šī procedūra var būt nepieciešama metastātiska kuņģa vēža gadījumā, pirms operācijas agrīnā stadijā vai lokāli izplatītā kuņģa vēža gadījumā. Ja audzējs traucē rīšanu, var nozīmēt staru terapiju, lai samazinātu tā izmēru.
Cilvēki ar kuņģa vēzi nereti saskaras ar asiņošanu – tas var būt saistīts gan ar pašu audzēju, gan ar tā ārstēšanu. Asiņošana var būt pēkšņa un īslaicīga (akūta) vai ilgstoša (hroniska). Asiņošanas apturēšanai ir vairākas metodes. To var ārstēt, ar endoskopa palīdzību ievadot medikamentus, apturot asiņošanu ar metāla klipšiem vai noslēdzot asiņojošo zonu ar karstuma palīdzību. Ja endoskopijas metodes nav efektīvas, var pielietot angiogrāfiju un embolizāciju: pa nelielu iegriezumu ādā asinsvadā tiek ievadīts katetrs jeb smalka plastikāta caurulīte, kontrolējot un uz vajadzīgo vietu to virzot ar rentgena palīdzību; kad asiņojošā vieta identificēta, radiologs bloķē (embolizē) asins plūsmu.
Ja audzējs rada spiedienu uz blakus esošajiem orgāniem vai cauraug nervus, var rasties stipras sāpes vēderā. Tās parasti ārstē ar dažāda veida pretsāpju līdzekļiem. Sāpes var mazināt arī paliatīvā staru terapija, kas ļauj samazināt audzēja izmēru. Atsevišķos gadījumos sāpes var atvieglot arī ķīmijterapija. Dažreiz nepieciešama kuņģa stenta izņemšana, ja tāds ticis lietots.
Audzēja radīts kuņģa vai barības vada nosprostojums var izraisīt sliktu dūšu, vemšanu, sāpes, svara zudumu un ēšanas grūtības. Ir ārstēšanas metodes, kas var palīdzēt mazināt šos simptomus un ļauj atgriezties pie normālas diētas, piemēram, operācija, ķīmijterapija un ārējā staru terapija. Ja audzējs nosprosto barības vadu vai vietu, kur barības vads savienojas ar kuņģi, var ievietot barības vada stentu jeb caurulīti, kas ļauj pārtikai nokļūt kuņģī. Ja audzējs nosprosto kuņģi un neļauj pārtikai nokļūt tievajā zarnā, var ievietot stentu, gastrostomijas zondi (G-tube) vai veikt gastrojejunostomiju, lai izveidotu jaunu “ceļu”, kā barībai apiet nosprostojumu.
Būtiska vēža ārstēšanas sastāvdaļa ir rehabilitācija. Tās mērķis ir sekmēt, lai cilvēks vēža ārstēšanas laikā un pēc tās varētu atgriezties ierastajā dzīvē un veikt ikdienas aktivitātes. Rehabilitācijas pakalpojumus sniedz multidiscpilināra speciālistu komanda, kurā parasti ietilpst psihologs, fizioterapeits, ergoterapeits, uztura speciālists, onkoloģiskās aprūpes māsa, arī mākslas vai mūzikas terapeits un sociālais darbinieks. Fizioterapija palīdz mazināt sāpes, stīvumu, nejutīgumu, kustību ierobežojumus vai citas fiziskās problēmas, kas radušās ārstēšanas rezultātā, savukārt ergoterapija palīdz atgūt spēju veikt ikdienas uzdevumus, sākot ar ģērbšanos vai ēst gatavošanu un beidzot ar atgriešanos darbā.
Ar vēža ārstēšanu saistītā noguruma, trauksmes, stresa, depresijas, bezpalīdzības pārvarēšanā atbalstu sniedz psihologs. Rehabilitācijas plāns tiek piemērots katram pacientam individuāli, atkarībā no funkcionēšanas traucējumu pakāpes. Vieglu vai mērenu funkcionēšanas grūtību gadījumā rehabilitācija parasti notiek ambulatori, smagāku funkcionēšanas traucējumu gadījumā rehabilitāciju nodrošina stacionārā.
Lasīt vairāk: Rehabilitācija>>
Pēc tam, kad visa nepieciešamā vēža ārstēšana ir pabeigta, pacients turpina atrasties onkologa uzraudzībā turpmākos piecus gadus. Šajā laikā būs regulāri jāveic izmeklējumi un jāapmeklē ārsts.
Vēža ārstēšana var izraisīt ilgtermiņa blakusparādības (tās, kas rodas ārstēšanas laikā vai īsi pēc tās un ilgst mēnešus vai gadus) un vēlākas blakusparādības (blakusparādības, kas rodas mēnešus vai gadus pēc slimības diagnosticēšanas vai ārstēšanas beigām). Tomēr blakusparādības parasti var kontrolēt gan ar medikamentiem, gan citām pieejām.
Regulāri tiks veikta kaulu blīvuma pārbaude, lai novērstu osteopēnijas un osteoporozes risku. Kaulu blīvuma samazināšanās ārstēšanai var būt nepieciešami medikamentus. Vēlams regulāri veikt D vitamīna līmeņa analīzes. Vienmēr nekavējoties jāziņo ārstam, ja parādās nebijuši simptomi vai ja pastiprinās līdzšinējie.

Latvijā, tāpat kā daudzās citās valstīs, nav kuņģa vēža skrīninga programmu, taču ārsts var ieteikt profilaktiskās pārbaudes – endoskopiju, attēldiagnostikas izmeklējumus, pepsinogēnu testu atrofiska gastrīta noteikšanai vai ureāzes elptestu h. pylori noteikšanai.

Lai samazinātu iespēju saslimt ar kuņģa vēzi, ieteicams:
- veikt h. Pylori testu un ārstēt, ja baktērija tiek atklāta;
- samazināt sāls patēriņu, tostarp ierobežojot arī dažādu kūpinātu vai marinētu produktu daudzumu uzturā;
- uzturā lietot galvenokārt augu valsts produktus;
- nesmēķēt;
- ierobežot alkohola patēriņu;
- būt fiziski aktīvam: Amerikas Vēža apvienības ieteikums vēža profilaksei ir vismaz 150 minūtes mērenas fiziskas aktivitātes nedēļā (piemēram, riteņbraukšana, peldēšana) vai vismaz 75 minūtes intensīvas fiziskas aktivitātes (piemēram, skriešana, aerobika, futbols, basketbols) nedēļā.
