


Olnīcu vēzis ir ļaundabīgs audzējs, kas veidojas olnīcās – reproduktīvajos orgānos, kas atbild par olšūnu un sievišķo hormonu ražošanu. Olnīcu vēzim ilgstoši var nebūt pamanāmu simptomu, turklāt, ja tos paciente sajūt, tie var līdzināties citu saslimšanu simptomiem.
Raksturīgākās šī vēža izpausmes ir vēdera uzpūšanās, diskomforts vai sāpes iegurnī, pilnuma sajūta vēderā, pietūkuši cirkšņu, padušu vai kakla rajona limfmezgli. Olnīcu vēža diagnosticēšanai visbiežāk izmanto ultrasonogrāfiju un datortomogrāfiju, kā arī asins analīzes. Agrīnas olnīcu vēža stadijas (I un II) nozīmē to, ka audzējs atrodas tikai olnīcās un tām tuvākajos audos, savukārt vēlīnās stadijās (III un IV) vēzis ir izplatījies attālākos vēdera dobuma orgānos vai plaušās.
Agrīnās stadijās olnīcu vēzis pamatā tiek ārstēts ķirurģiski, vēlīnākās stadijās papildus ķirurģijai visbiežāk lieto ķīmijterapiju; staru terapiju, mērķterapiju un hormonterapiju izvēlas specifiskos gadījumos. Iespēju saslimt ar olnīcu vēzi palielina ģenētiskās mutācijas, vecums, aptaukošanās, kā arī krūts, olnīcu, dzemdes un kolorektālā vēža gadījumi ģimenē.

Starp ļaundabīgajiem audzējiem olnīcu vēzis ir īpaši izaicinošs, jo tas bieži attīstās nemanāmi. Audzējs veidojas olnīcās – sievietes reproduktīvajos orgānos, kas ražo olšūnas un hormonus. Slimības sākumstadijā simptomi parasti ir nespecifiski vai vāji izteikti, tāpēc olnīcu vēzi nereti atklāj vēlīni. Tas apgrūtina ārstēšanu un var ietekmēt dzīvildzi (dzīvildze – laiks, ko cilvēks nodzīvo pēc diagnozes noteikšanas).
Latvijā aptuveni divas trešdaļas no visiem ļaundabīgajiem olnīcu audzējiem tiek atklāti slimības III un IV stadijā.1 Pirmajās divās stadijās to parasti diagnosticē nejauši – ārstējot kādu citu slimību, piemēram, veicot žultspūšļa vai aklās zarnas operāciju. Visbiežāk olnīcu vēzi sievietēm atklāj pēc tam, kad iestājusies menopauze – pēc 50–55 gadu vecuma, kad izmainās olnīcu darbība un samazinās estrogēna daudzums. Tomēr no šīs slimības nav pasargātas arī gados jaunas sievietes. Latvijā ik gadu atklāj aptuveni 300 jaunu olnīcu vēža gadījumu.2
Olnīcu audzēja veidošanās un izplatīšanās
Olnīcu audzējs var attīstīties pašā olnīcā vai tuvējās struktūrās – piemēram, olvadā vai vēdera dobumā (vēderplēvē). Audzēja veids ir atkarīgs no tā, kuras šūnas sāk nekontrolēti dalīties.
Olnīcā ir trīs galvenie šūnu veidi:
Olnīcu vēzis bieži izplatās vēdera dobumā. Tas var skart tuvumā esošos audus un orgānus – vēderplēvi, taukplēvi, zarnas, aknas, kuņģi un diafragmu. Slimība var izplatīties arī ar asinsriti vai limfātisko sistēmu uz attālākiem orgāniem, piemēram, plaušām vai smadzenēm. Olvados vēzis biežāk nonāk no citas vietas – visbiežāk no olnīcas vai dzemdes gļotādas (endometrija). Retāk olvados primāri attīstās jauns audzējs.
Precīza audzēja sākotnējās (primārās) atrašanās vietas noteikšana ir ļoti svarīga, jo tā palīdz ārstiem izvēlēties piemērotāko ārstēšanas stratēģiju un prognozēt slimības gaitu.3 Olnīcu audzēju veidu nosaka atkarībā no tā, kura veida olnīcu veidojošajās šūnās rodas audzējs. Tā kā olnīca sastāv no ļoti dažādām šūnām, olnīcu audzējiem ir ap 200 histoloģisko variantu – šādas dažādības nav nevienas citas lokalizācijas vēzim.

Olnīcu vēzim parasti nav izteiktu agrīnu pazīmju. Šie audzēji parasti aug strauji un reti izraisa sāpes vai citus simptomus, kas ļautu tos savlaicīgi pamanīt.

Olnīcu vēzim parasti nav izteiktu agrīnu pazīmju. Šie audzēji parasti aug strauji un reti izraisa sāpes vai citus simptomus, kas ļautu tos savlaicīgi pamanīt. Tā kā tas bieži netiek atklāts līdz pat vēlīnām stadijām, tā ārstēšana ir sarežģīta.
Olnīcu vēzis var izraisīt šādus simptomus:

Precīzs olnīcu vēža rašanās iemesls pagaidām nav skaidrs, taču ir zināmi vairāki faktori, kas ievērojami palielina risku saslimt ar šo audzēju.

Neietekmējamie (nemodificējamie) riska faktori:
Ietekmējamie (modificējamie) riska faktori:

Tiek aktīvi pētītas olnīcu vēža skrīninga iespējas, kā atklāt olnīcu vēzi agrīni, piemēram, veicot asins analīzi CA125 un ginekoloģisko ultrasonogrāfiju pēcmenopauzes vecuma sievietēm. Tomēr līdz šim pētījumi nav pierādījuši, ka šīs metodes būtu pietiekami efektīvas agrīnai atklāšanai. Tāpēc šobrīd olnīcu vēzim nav valsts skrīninga programmas.

Vāji izteikto agrīno pazīmju vai pat to trūkuma dēļ olnīcu vēzis bieži tiek atklāts salīdzinoši vēlīnā stadijā – aptuveni 60 % sieviešu, kurām diagnosticēts olnīcu vēzi, diagnozes noteikšanas brīdī slimība ir progresējusi.15 Latvijā aptuveni divas trešdaļas no visiem ļaundabīgiem epiteliālajiem olnīcu audzējiem tiek diagnosticēti slimības III un IV stadijā.16
Vienmēr, parādoties aizdomām par ļaundabīgām izmaiņām olnīcās, nekavējoties jāvēršas pie speciālista – onkologa vai onkoloģijas ginekologa. Ja ultrasonogrāfijā atklāj olnīcu veidojumu, sievietei vispirms nosaka audzēju biomarķierus asinīs. Ja rādītāji ir paaugstināti, tiek veikta vēdera dobuma un mazā iegurņa datortomogrāfija ar kontrastvielu. Šos izmeklējumus organizē “zaļā koridora” ietvaros. Datortomogrāfija palīdz precīzāk izvērtēt, vai veidojums ir labdabīgs vai ļaundabīgs, un, ja tas ir vēzis, palīdz plānot operācijas apjomu.
Par jebkuru izmeklējumu nepieciešamību lemj ārsts, kas specializējies olnīcu vēža ārstēšanā un diagnostikā.
Klīniskās izmeklēšanas laikā olnīcu vēzi nereti var konstatēt pēc šādām, parasti vāji izteiktām, pazīmēm:
Vizuālā diagnostika, kas piemērota olnīcu vēža gadījumā:
Kā sagatavoties radioloģiskajiem izmeklējumiem un kādas var būt to blaknes? Lasi ŠEIT!
Biomarķieri ir bioloģiskas molekulas, kas var liecināt par vēža klātbūtni organismā. Tās ražo vai nu pats audzējs, vai organisma veselās šūnas, reaģējot uz audzēju. Vienlaikus jāatceras, ka biomarķieru līmeni var ietekmēt arī ar audzēju nesaistīti procesi.
Olnīcu vēža gadījumā tiek pievērsta uzmanība šādiem biomarķieriem:
Līdz šim par nozīmīgāko laboratorisko rādītāju olnīcu vēža diagnostikā uzskata audzēja marķieri CA125, kā arī CA125 un HE4 kombināciju. Abu šo biomarķieru rezultātus izvērtē, izmantojot ROMA algoritmu (Risk of Ovarian Malignancy Algorithm). Tas palīdz noteikt, kurām sievietēm pastāv augsts ļaundabīga olnīcu audzēja risks un nepieciešama tālāka izmeklēšana un konsultācija pie onkoginekologa.23
ROMA rezultāti vienmēr jāvērtē kopā ar klīnisko ainu un radioloģisko izmeklējumu datiem – tie nav interpretējami izolēti.
Atsauces vērtības atšķiras sievietēm pirms un pēc menopauzes:
Pastāv arī citi riska kalkulatori, taču ROMA algoritms ir viens no visbiežāk izmantotajiem klīniskajā praksē.24

Olnīcu vēža stadijas tiek klasificētas pēc FIGO (Starptautiskā Ginekologu un dzemdību speciālistu federācija, Federation Internationale de Gynecolgie et d'Obstetrique) stadiju noteikšanas sistēmas, kas izstrādāta tieši ginekoloģiskās sistēmas audzējiem.

Olnīcu vēža stadijas tiek klasificētas pēc FIGO (Starptautiskā Ginekologu un dzemdību speciālistu federācija, Federation Internationale de Gynecolgie et d'Obstetrique) stadiju noteikšanas sistēmas, kas izstrādāta tieši ginekoloģiskās sistēmas audzējiem. Ginekoloģiskajiem audzējiem, tajā skaitā olnīcu vēzim, ir četras stadijas, kuras apzīmē ar romiešu cipariem no I līdz IV – jo mazāks stadiju apzīmējošais skaitlis, jo mazāk audzējs ir izplatījies un jo labāka ir audzēja ārstēšanas prognoze. Visprecīzāk šī vēža stadiju nosaka ķirurģiski, pēc operācijas materiāla histoloģiskas izanalizēšanas. Tomēr ja audzējs ir ļoti izplatījies, lielāka nozīme būs attēlizmeklējumiem.
Olnīcu vēža stadijas25:


Olnīcu vēža 5 gadu dzīvildzes (nodzīvotie gadi pēc diagnozes atklāšanas) rādītājs ir atkarīgs no dažādiem faktoriem, piemēram, no vēža stadijas, pacienta vecuma, vispārējā veselības stāvokļa un no tā, vai vēzis ir diagnosticēts nesen vai arī ir atgriezies (recidivējis).

Visbiežāk nosaka piecu gadu dzīvildzes līmeni – tādu saslimušo īpatsvaru, kuri ir dzīvi piecus gadus pēc diagnozes apstiprināšanas. Kopumā dzīvildzes jeb izdzīvotības rādītāji olnīcu vēža gadījumā ir ievērojami zemāki nekā citu vēža veidu, piemēram, krūts vēža, gadījumā. Zemāka dzīvildze lielā mērā ir vāji izteikto simptomu dēļ, kas ir iemesls vēlīnai olnīcu audzēja atklāšanai. Tāpat arī dzīvildze būtiski atšķiras dažādām audzēja stadijām un histoloģiskajiem tipiem.
Dzīvildzes statistika balstās uz lielu cilvēku grupu datiem, tāpēc nevar precīzi paredzēt, kas notiks ar katru konkrētu pacientu. Šie rādītāji sniedz tikai vispārīgu priekšstatu par slimības gaitu, nevis individuālu prognozi. Piemēram, cilvēkam ar labu kopējo veselību un bez citām nopietnām slimībām prognoze var būt labāka nekā vidējie statistikas dati. Jāņem vērā arī tas, ka dzīvildzes rādītāji parasti balstās uz pacientiem, kuri diagnosticēti pirms vismaz pieciem gadiem. Tas nozīmē, ka jaunākās ārstēšanas metodes šajos datos vēl var nebūt pilnībā atspoguļotas.
5 gadu dzīvildzes rādītāji, kas aprēķināti, balstoties 2012. –2018.gada statistikā, ir šādi:
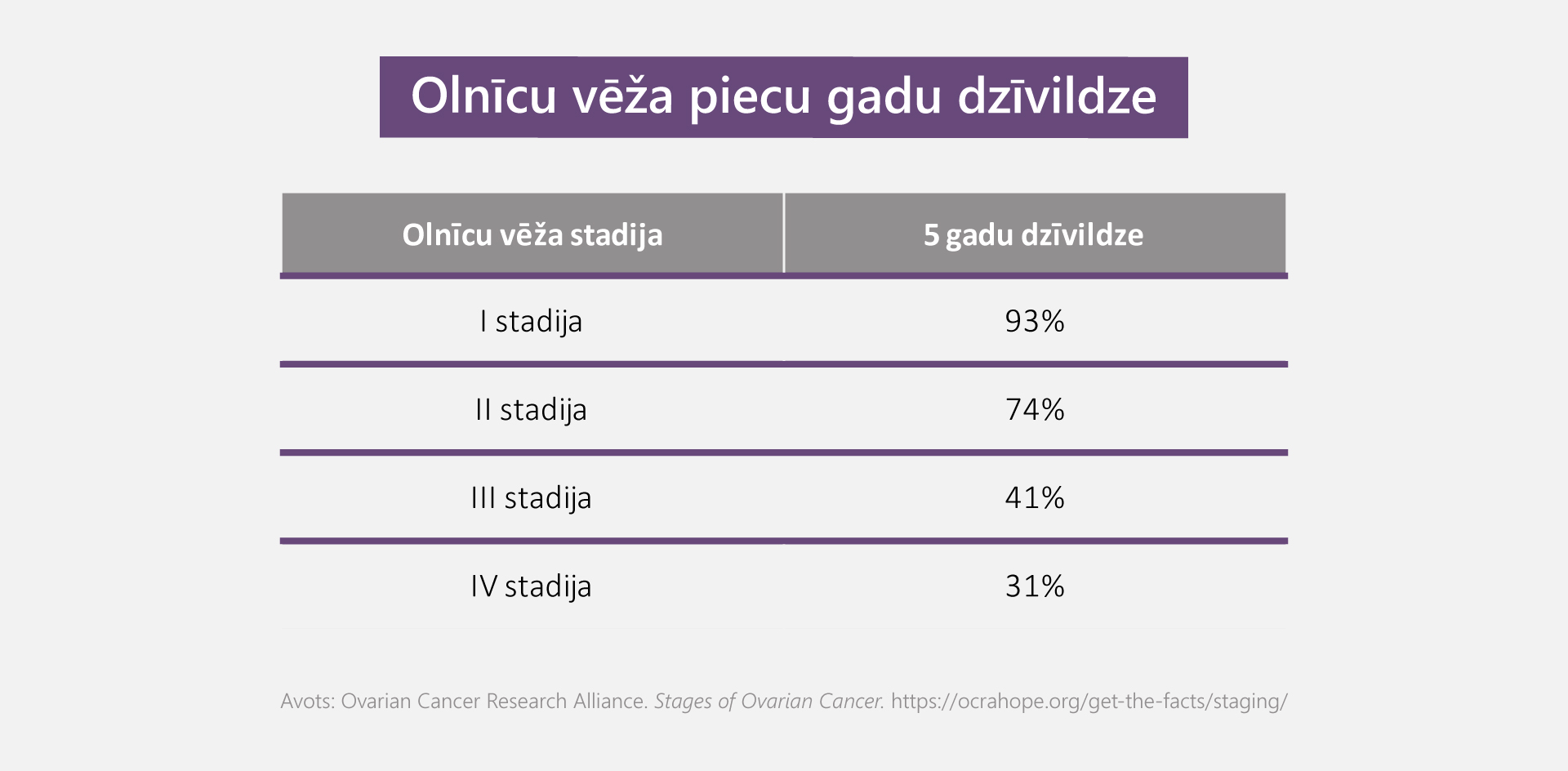
*26
Lai arī pirmajai un otrajai slimības stadijai dzīvildze atšķiras no trešās un ceturtās stadijas, tomēr arī trešajā un ceturtajā stadijā pēc ķīmijterapijas ir ļoti lielas iespējas izārstēties, jo olnīcu vēzis ir ļoti jutīgs pret ķīmijterapiju. Arī pateicoties ķirurģisko metožu pilnveidei un efektīvākiem inovatīvajiem medikamentiem, olnīcu vēža slimnieču dzīvildze pēdējo 20 gadu laikā ir palielinājusies, un olnīcu vēzi jau var pielīdzināt hroniskai ārstējamai slimībai.

Drošticamas olnīcu vēža ārstēšanas vadlīnijas izdevusi gan viena no Eiropas vadošajām profesionālajām organizācijām onkoloģijā (angļu valodā) – Eiropas Onkologu ķīmijterapeitu biedrība (European Society For Medical Oncology, ESMO), gan ASV Nacionālais visaptverošais vēža tīkls (National Comprehensive Cancer Network, NCCN).

ESMO epiteliālā olnīcu vēža ārstēšanas vadlīnijas angļu valodā lasāmas: ŠEIT
ESMO neepiteliālā olnīcu vēža ārstēšanas vadlīnijas lasāmas: ŠEIT
NCCN olnīcu vēža diagnostikas, stadijas noteikšanas un ārstēšanas vadlīnijas pacientiem angļu valodā lasāmas: ŠEIT
Olnīcu vēža ārstēšana ir atkarīga no audzēja stadijas un tā izplatības organismā. Galvenie ārstēšanas veidi ir ķirurģiska operācija un ķīmijterapija – tie veido pamatu sekmīgai ārstēšanai. Pirms lēmuma pieņemšanas par piemērotāko terapiju tiek veikti radioloģiskie un laboratoriskie izmeklējumi, dažkārt arī diagnostiska laparoskopija. Pēc tam situāciju izvērtē onkoginekologu un radiologu konsīlijs, kas lemj par primāras radikālas operācijas iespēju.
Par primāru ārstēšanu sauc sākotnējo, konkrētajam vēža veidam ieteicamo ārstēšanas metodi, bet radikāla ārstēšana nozīmē, ka tās mērķis ir pilnīga slimības izārstēšana, nevis tikai simptomu mazināšana. Ja audzējs nav plaši izplatījies, ārstēšanu parasti sāk ar operāciju. Izoperētais audu materiāls tiek nosūtīts patohistoloģiskai izmeklēšanai – patologs mikroskopiski izvērtē vēža šūnas, nosakot audzēja tipu un agresivitāti. Patologa slēdziens ir viens no būtiskākajiem diagnozes precizēšanas posmiem, jo tas ietekmē turpmāko ārstēšanas plānu un prognozi.
Atkarībā no slimības stadijas ārstu konsīlijs lemj par tālāko terapiju. Agrīnās stadijās pēc radikālas operācijas dažkārt pietiek ar regulāru onkoginekoloģisku novērošanu. Ja audzējs ir agresīvāks vai izplatītāks, pēc operācijas tiek nozīmēta adjuvanta (pēcoperācijas) ķīmijterapija, lai mazinātu risku, ka audzējs atgriežas. Onkologs ķīmijterapeits, ņemot vērā operācijas apjomu, histoloģiskos rezultātus un slimības stadiju, izvēlas piemērotāko ārstēšanas shēmu. Ja audzējs ir plaši izplatījies un primāra radikāla operācija nav iespējama, ārstēšanu sāk ar neoadjuvantu (pirmsoperācijas) ķīmijterapiju. Tās mērķis ir samazināt audzēja apjomu un padarīt turpmāko operāciju iespējamu un efektīvāku.
Olnīcu vēža gadījumā ir svarīgi precīzi izvērtēt, vai audzēju iespējams ķirurģiski operēt. Operācijas mērķis ir ķirurģiski izņemt visu redzamo audzēja masu – no tā, cik izdevusies šī operācija, ir atkarīga tālākā slimības prognoze un dzīvildze. Arī pēc radikālas operācijas nereti nozīmē adjuvantu jeb pēcoperācijas ķīmijterapiju.
Lai ķirurģiski izoperētu audzēja masu, parasti tiek veikta laparotomija jeb konvencionāla tipa operācija (vēdera dobuma atvēršana ar plašu griezienu, kas var sniegties no krūšu kurvja lejasdaļas līdz pat mazajam iegurnim). Savukārt laparoskopisku operāciju, kad vairākās vietās vēdera sienā tiek izdarīti nelieli iegriezumi apmēram 1 cm garumā, visbiežāk veic diagnostiskos nolūkos vai agrīnas stadijas audzēja gadījumā.
Atkarībā no audzēja izplatības pakāpes, var veikt dažāda apmēra bojāto orgānu operāciju:
Ķirurģiskas operācijas laikā var veikt arī iegurņa dobuma skalošanu – tā ir diagnozi precizējoša procedūra, kuras laikā vēdera dobums tiek izskalots ar fizioloģisko šķīdumu, un iegūtais materiāls tiek nosūtīts citopatoloģiskai novērtēšanai. Šīs procedūras mērķis ir noskaidrot, vai audzēja šūnas nav izplatījušās iegurņa dobumā, tā var arī palīdzēt atklāt ļaundabīgus veidojumus, kurus neizdodas konstatēt operācijas laikā.
Sievietēm reproduktīvā vecumā var veikt auglību saglabājošu operāciju, ja vien to pieļauj audzēja raksturs un attīstības stadija; iespējamas arī tādas auglību saglabājošas procedūras kā, piemēram, olšūnu iesaldēšana. Olšūnu paņemšanu, sasaldēšanu un uzglabāšanu uz laiku līdz 10 gadiem apmaksā no valsts budžeta, ja šīs procedūras nepieciešamību pamato ārstu konsīlija lēmums.
Auglību saglabājoša ķirurģija olnīcu vēža gadījumā ir iespējama, ja audzējs nav skāris dzemdi un vismaz vienu no olvadiem. Lielākas iespējas saglabāt auglību ir neepitēlijšūnu audzēja, sevišķi germinatīvo šūnu vēža, kā arī agrīnas slimības stadijas gadījumā.28 Olšūnu sasaldēšana būtu jāveic pirms ķīmijterapijas, jo auglību ietekmē ne tikai operācijas veids, bet arī ķīmijterapija, kura nereti bojā atlikušo olvadu un paātrina menopauzes iestāšanos.
Auglību saglabājošās ķirurģijas iespējas atšķirīgiem olnīcu vēža paveidiem dažādās stadijās apskata 2021. gadā publicēts sistemātiskais pārskats “Fertility-Sparing Surgery for Ovarian Cancer” (“Auglību saudzējoša olnīcu vēža ķirurģija”), kas apkopo secinājumus no publikācijām MEDLINE, PubMed, Cochrane Library un Cochrane datubāzēs.
Kā jau pēc jebkuras operācijas, arī pēc olnīcu vēža operācijas pastāv komplikāciju risks. Daudzas komplikācijas ir viegli ārstējamas un novēršamas, bet dažas var būt dzīvībai bīstamas.
Biežāk sastopamie pēcoperācijas sarežģījumi ir šādi:29
Operācijas grieziens var būt plašs – tas var stiepties no kaunuma apmatojuma līdz nabai vai virs tās, dažkārt pat līdz krūškurvja apakšējai daļai.Pēc operācijas vēdera dobumā var ievietot drenas – elastīgas caurulītes, kas palīdz novadīt šķidrumu. Parasti tās izņem dažu dienu laikā. Urīna novadīšanai īslaicīgi var tikt ievietots urīnpūšļa katetrs.
Pirmajā nedēļā pēc operācijas iespējamas sāpes brūces apvidū, tādēļ var būt nepieciešami pretsāpju līdzekļi, arī intravenozas infūzijas veidā. Ēst un dzert drīkst atsākt, kad to atļauj ārsts un atjaunojas pašsajūta – tas ir atkarīgs no operācijas apjoma.Ieteicams pēc iespējas ātrāk sākt kustēties, ja iespējams – jau operācijas dienā.
Svarīgi veikt arī kāju vingrinājumus, lai mazinātu trombu veidošanās risku. Vairākas nedēļas jāizvairās no smagumu celšanas un darbībām, kas noslogo vēdera muskuļus (piemēram, smagu iepirkumu maisiņu nešana vai intensīva mājas uzkopšana).Pēc operācijas būs nepieciešamas regulāras vizītes pie onkoginekologa un kontroles izmeklējumi – asins analīzes, ultrasonogrāfija, datortomogrāfija. Laika gaitā pārbaužu biežums samazināsies, un to noteiks ārstējošais ārsts.30
Ķīmijterapija ir vēža ārstēšana ar medikamentiem, kas iznīcina vēža šūnas, apturot to augšanu vai vairošanos. Dažādi medikamenti iedarbojas uz atšķirīgām šūnas dzīves cikla fāzēm, bet mērķis ir viens – apstādināt audzēja augšanu un novērst slimības tālāku progresu. Ar ķīmiskajiem preparātiem var tikt bojātas arī veselas šūnas, īpaši tās, kas ātri dalās, tomēr šīs šūnas pēc ķīmijterapijas parasti atjaunojas. Parasti ķīmijterapiju ievada intravenozi (līdzekļa ievadīšana vēnā), taču atsevišķi medikamenti ir arī tablešu un kapsulu formā.
Ķīmijterapijas ievadīšanas ceļš var būt arī intraperitoneāls – līdz noteiktai temperatūrai sasildīta ķīmijterapijas līdzekļa ievadīšana vēdera dobumā ar speciālas iekārtas palīdzību). Lai arī intraperitoneālo ķīmijterapiju (HIPEC, hyperthermic intraperitoneal chemotherapy) atsevišķos gadījumos veic arī Latvijā, tomēr pagaidām šī metode tiek vērtēta pretrunīgi – pētījumi par tās priekšrocībām vēl joprojām turpinās.
Nepieciešamo ķīmijterapijas ciklu skaits var atšķirties atkarībā no konkrētas situācijas: piemēram, slimības II stadijā parasti tiek nozīmēti 3–6 kursi.31
Ķīmijterapiju var lietot pirms ķirurģiskas operācijas (neoadjuvanti) vai pēc tās (adjuvanti). Pirmsoperācijas ķīmijterapiju veic, lai samazinātu audzēju, savukārt pēcoperācijas jeb adjuvanta ķīmijterapija palīdz iznīcināt vēža šūnas, kas palikušas pēc operācijas. Ja ķirurģiska ārstēšana nav iespējama (piemēram, vēlīnās audzēja stadijās), ķīmijterapiju lieto paliatīvi – lai stabilizētu audzēju un mazinātu simptomus.
Olnīcu vēža gadījumā visbiežāk izmantotie ķīmijterapijas preparāti ir platīna bāzes preparāti (cisplatīns, karboplatīns) vai taksāni (paklitaksels, docetaksels). Latvijā šobrīd ir pieejami medikamenti visām stadijām: visbiežāk piemēro kombinētu ķīmijterapiju ar paklitakselu vai docetakselu kopā ar karboplatīnu.32
Visvairāk pierādījumu ir par karboplatīna efektivitāti. Visām sievietēm ar olnīcu vēzi II, III vai IV stadijā standarta ārstēšana tiek veikta ar paklitakselu un karboplatīnu intravenozi reizi trijās nedēļās, parasti veicot sešus šādus ciklus. Sievietēm, kas nepanes paklitakselu, tas tiek aizvietots ar docetakselu vai pegilētu liposomālo doksorubicīnu.33
Olnīcu vēža ārstēšana tiek plānota pakāpeniski. Katru nākamo sistēmiskās ārstēšanas posmu sauc par terapijas līniju. Tas nozīmē, - ja slimība atgriežas vai progresē, tiek izvēlēta nākamā ārstēšanas līnija, kas var tikt kombinēta ar citām ārstēšanas metodēm, piemēram, ķirurģiju. Ārstēšanas plāns tiek izvēlēts saskaņā ar starptautiskām vadlīnijām un valstī pieejamām metodēm.34 35
1. līnijas sistēmiska terapija
Tā ir pirmā sistēmiskā ārstēšana pēc diagnozes noteikšanas.
Olnīcu vēža ārstēšana tiek plānota pakāpeniski. Katru nākamo sistēmiskās ārstēšanas posmu sauc par terapijas līniju. Tas nozīmē, - ja slimība atgriežas vai progresē, tiek izvēlēta nākamā ārstēšanas līnija, kas var tikt kombinēta ar citām ārstēšanas metodēm, piemēram, ķirurģiju. Ārstēšanas plāns tiek izvēlēts saskaņā ar starptautiskām vadlīnijām un valstī pieejamām metodēm.34 35
2. līnijas sistēmiska terapija
To pielieto , ja slimība atgriežas pēc pirmās ārstēšanas vai pirmās līnijas ārstēšana bijusi nesekmīga un audzējs nav reaģējis uz ārstēšanu.
Ārstēšanas izvēle galvenokārt atkarīga no tā, cik ātri slimība atgriezusies (recidivējusi):
3. līnijas un turpmāku līniju sistēmiska terapija
Ja slimība progresē arī pēc 2. līnijas terapijas, tiek izvēlēta nākamā – 3. līnijas terapija.
Šajā posmā ārsti rūpīgi izvērtē:
Šie rādītāji tiek atkārtoti izvērtēti pirms katras jaunas terapijas līnijas.
Dažkārt iespējama dalība klīniskajos pētījumos vai tiek izvēlēta ārstēšana, kuras galvenais mērķis ir simptomu mazināšana un dzīves kvalitātes saglabāšana. 49
Ķīmijterapijas medikamenti iedarbojas ne tikai uz vēža šūnām, bet arī uz veselajām šūnām – pārsvarā tādām, kurām raksturīga aktīva dalīšanās: kaulu smadzeņu šūnas, gremošanas trakta epitēlijšūnas, dzimumšūnas, šūnas matu saknēs u.tml.
Blakusparādības attīstās ļoti individuāli un neskar visus vienādi. Blakusparādības attīstās ļoti individuāli un neskar visus vienādi. Vairums pacientu jūtas ļoti noguruši, raksturīga psiholoģiska nomāktība, mainās asins analīžu rādītāji, var pastiprināties matu izkrišana, ir slikta dūša, šķebināšana. Vemšana sastopama samērā reti, tādos gadījumos tiek nozīmēta pretvemšanas medikamenti. Dažreiz slikta dūša nav saistīta tikai ar ķīmijterapiju, iemesls var būt arī pats audzējs, pretsāpju līdzekļu blakusparādības un citi iemesli.
Pēc ķīmijterapijas kursa var būt paaugstināta temperatūra, kuras gadījumā nekavējoties jāvēršas pie ģimenes ārsta vai jāpiesaka ģimenes ārsta mājas vizīte, kā arī laboratorijā jāveic asins analīzes, lai noteiktu leikocītu līmeni asinīs. Ja papildus paaugstinātai ķermeņa temperatūrai parādās arī citi simptomi, nekavējoties jāvēršas slimnīcas uzņemšanas nodaļā.
Ķīmijterapijas kursa laikā var rasties arī nagu bojājumi, plaukstu–pēdu sindroms, stomatīts (mutes gļotādas iekaisums). Jo ilgāk pacients saņem terapiju, jo blakusparādību iespējas ir lielākas – tām parādoties, nekavējoties jāvēršas pēc palīdzības pie ārsta. Lai arī ķīmijterapija parasti pieprasa dzīvesveida korekcijas, tomēr, ja pašsajūta atļauj, ir iespējams gan turpināt strādāt, gan saglabāt sociālo aktivitāti.
Ja ķīmijterapijā tiek kombinēti vairāki medikamenti, blakusparādību risks var būt lielāks un tās var parādīties vienlaikus. Lietojot vienu preparātu, blakusparādības parasti ir mazāk izteiktas, taču tas atkarīgs no konkrētajām zālēm un organisma reakcijas.Ķīmijterapija var ietekmēt asinsradi – īpaši samazināt leikocītu (balto asinsķermenīšu) skaitu.
Tas var izraisīt:
Šādos gadījumos palielinās infekciju risks, un tās var būt arī nopietnas vai pat dzīvībai bīstamas.Iespējamās pazīmes, kurām jāpievērš uzmanība:
Ja parādās drudzis (īpaši temperatūra virs 38 °C) vai citas infekcijas pazīmes, nekavējoties jāsazinās ar ārstējošo ārstu.
Organisma spēju cīnīties ar infekcijām nosaka leikocītu (balto asinsķermenīšu) absolūtais skaits asinīs. Par leikopēniju runā, ja kopējais leikocītu skaits ir zem 3,0 × 10⁹/l.Par neitropēniju – ja neitrofilo leikocītu (šūnu, kas īpaši svarīgas cīņā ar bakteriālām infekcijām) absolūtais skaits ir mazāks par 2,0 × 10⁹/l. Ķīmijterapijas izraisīta neitropēnija dažkārt var būt iemesls atlikt vai pārcelt nākamo ārstēšanas ciklu. Lai novērtētu komplikāciju risku, ārsti var izmantot MASCC (Multinational Association for Supportive Care in Cancer) izstrādāto riska skalu.
Ja pastāv paaugstināts neitropēnijas risks, profilaksei vai ārstēšanai tiek nozīmēti medikamenti – granulocītu koloniju stimulējošie faktori (G-CSF), piemēram, pegfilgrastims vai lipegfilgrastims. Tie palīdz kaulu smadzenēm ātrāk atjaunot leikocītu skaitu. Leikopēnijai un neitropēnijai pašām par sevi parasti nav izteiktu simptomu, tādēļ tās regulāri kontrolē ar asins analīzēm. Tomēr šo stāvokļu dēļ organisms kļūst uzņēmīgāks pret infekcijām, kas var izpausties ar dažādām pazīmēm, tostarp paaugstinātu ķermeņa temperatūru, drebuļiem, kakla sāpēm vai vispārēju nespēku. Ja parādās drudzis, nekavējoties jāsazinās ar ārstu.
Var attīstīties ar limfopēnija jeb limfocītu samazināšanās. Šādos gadījumos nereti var parādīties herpes infekcijas (Herpes simplex 1 un 2) izpausmes, piemēram, “aukstumpumpas”, herpes izsitumi degunā, vai arī vējbaku izraisītāja (Varicella zoster vīruss) izpausmes – jeb tā sauktā “jostas roze”. Herpes vīrusu gadījumā ar tik nozīmēta papildus ārstēšana ar pretvīrusu zālēm.
Izplatīta vēža blakusparādība ir anēmija – nepietiekams sarkano asinsķermenīšu (eritrocītu) skaits vai pazemināts hemoglobīna līmenis, kas pavājina organisma apgādi ar skābekli. Anēmiju izraisa gan noteikti vēža veidi paši par sevi, tostarp olnīcu vēzis, gan arī atsevišķi ķīmijterapijas preparāti, piemēram, platīna preparāti.50 Smagākos gadījumos var būt nepieciešama asins pārliešana. Ar anēmiju bieži saistāma astēnija jeb izteikts psihisks un fizisks nespēks, viegla nogurdināmība.
Trombocitopēnija (samazināts trombocītu skaits). Trombocitopēnija var būt iemesls asiņošanām, kas var izpausties gan kā sīki zemādas asinsizplūdumi, pastiprināta zilumu veidošanās, sārti iekrāsojies urīns, tumšas vai asiņainas fēces, asiņošana no deguna, smaganām un dzimumceļiem.51 Smagākos gadījumos var būt nepieciešama asins pārliešana.
Perifērā neiropātija – nervu šķiedru bojājums, kas var izpausties kā tirpšana, durstīšana, dedzinoša vai saldējoša sajūta roku un kāju pirkstos, līdzsvara traucējumi, grūtības paņemt un noturēt rokās sīkus priekšmetus vai veikt sīkas darbības ar pirkstiem; var būt arī stīvuma sajūta mēlē vai grūtības norīt un runāt. Reizēm periferiālā neiropātija izpaužas arī ar sāpēm žokļos, vēderā, dzirdes pasliktināšanos vai aizcietējumu, ko rada bojāti zarnu kustīgumu nodrošinošie nervi. Parasti lielākā daļa šādu sūdzību pēc ķīmijterapijas beigām pāriet, taču var būt nepieciešama ķīmijterapijas līdzekļa maiņa.52
Šobrīd nav pārliecinošu efektīgu līdzekļu perifēras neiropātijas novēršanai un ārstēšanai, taču pētījumi turpinās. Viena no metodēm ķīmijterapijas izraisītas perifērās neiropātijas mazināšanai ir krioterapija (hipotermija) – roku (vai pēdu) turēšana aukstumā infūzijas laikā, lai samazinātu zāļu ietekmi uz nerviem viena no metodēm ir krioterapijas vai hipotermija - jeb turēt rokas aukstumā taksānu terapijas laikā, lai samazinātu zāļu ietekmi uz nerviem.53
Mukozīts (iekaisīgs gļotādu bojājums) visbiežāk skar mutes un rīkles gļotādu, izraisot stomatītu, kā rezultātā ir apgrūtināta barības košļāšana un rīšana, nereti arī runāšana. Ļoti bieži mukozīts iet kopsolī ar samazinātu siekalu izdalīšanos un mutes sausumu. Šī ir izplatīta ķīmijterapijas blakusparādība, tomēr tā var neparādīties visiem. 54
Alopēcija (matu izkrišana) – bieža, taču parasti īslaicīga ķīmijterapijas blakusparādība. Tā raksturīga daudziem, bet ne visiem medikamentiem, un biežāk novērojama, lietojot taksānu un antraciklīnu grupas ķīmijterapiju.Var izkrist ne tikai galvas mati, bet arī uzacis un skropstas. Skropstu izkrišana var palielināt acu kairinājuma un iekaisuma risku, savukārt deguna matiņu zudums var veicināt biežāku iesnu vai deguna gļotādas jutīgumu.Parasti mati sāk ataugt dažus mēnešus pēc ārstēšanas beigām, lai gan sākumā tie var būt citādas struktūras vai krāsas.
Caureja – tās laikā organisms zaudē ūdeni, tādēļ, lai izvairītos no ķermeņa atūdeņošanās, svarīgi uzņemt pietiekami daudz – vismaz astoņas glāzes – negāzēta un nesaldināta šķidruma dienā. Uzturā vēlams lietot produktus ar zemu šķiedrvielu daudzumu un, ja iespējams, ar augstu kālija saturu (piemēram, kartupeļi, banāni, apelsīni).55
Citas salīdzinoši izplatītas ķīmijterapijas blaknes ir anoreksija (vāja apetīte vai tās pilnīgs trūkums), t.s. plaukstu-pēdu ādas reakcija jeb palmāri plantārās eritrodizestēzijas sindroms – plaukstu un pēdu ādas iekaisums (apsārtums, čūlošana) un to nejutīgums, tūska (šķidruma uzkrāšanās ķermeņa audos), elpas trūkums.56
Kā sagatavoties ķīmijterapijai lasiet: ŠEIT.
Staru terapija ir ārstēšanas metode, kurā izmanto augstas enerģijas jonizējošo starojumu (piemēram, rentgena vai gamma starus), lai iznīcinātu vēža šūnas vai samazinātu audzēja izmēru.
Starojumu var ievadīt dažādos veidos:
Ārstēšanas veidu izvēlas ārsts, ņemot vērā audzēja tipu, atrašanās vietu un slimības stadiju. Bieži vien staru terapija tiek kombinēta ar ķīmijterapiju un tiek piemērota pēc operācijas, lai nodrošinātu, ka tiek iznīcinātas visas vēža šūnas. Taču olnīcu vēža gadījumā staru terapiju nepiemēro bieži – to izvēlas galvenokārt recidivējoša (ar tendenci atkārtoties) vai metastātiskas epitēlija olnīcu vēža ārstēšanai.57
Par staru terapju vairāk lasiet: ŠEIT.
Staru terapija ir lokāla ārstēšanas metode, kas nozīmē, ka tā iedarbojas uz konkrētu apstaroto ķermeņa zonu. Līdz ar to arī blakusparādības parasti ir saistītas tieši ar šo zonu.
Ārstējot olnīcu vai citus ginekoloģiskos audzējus ar staru terapiju, biežāk var novērot:
Blakusparādības parasti sākas apmēram nedēļu pēc terapijas uzsākšanas, ārstēšanas laikā var pastiprināties un saglabāties vēl dažas nedēļas pēc kursa beigām.
Pašsajūtas uzlabošanai ieteicams:
Ja simptomi kļūst izteikti vai traucē ikdienas dzīvi, par to jāinformē ārstējošais ārsts.
Par staru terapijas blakusparādībām vairāk lasiet: ŠEIT.
Hormonterapija ir ārstēšanas metode, kuras mērķis ir samazināt, bloķēt vai iznīcināt noteiktu hormonu iedarbību organismā, lai palēninātu vai apturētu dažu hormonu jutīgu audzēju (piemēram, krūts vai prostatas vēža) augšanu.
Terapijā var izmantot:
Olnīcu vēža gadījumā hormonterapija nav standarta ārstēšanas metode. Tomēr dažos retos olnīcu audzēju veidos vai situācijās, kad citas ārstēšanas metodes nav bijušas efektīvas, ārsts var apsvērt arī hormonālās terapijas iespēju.
Mērķterapija ir ārstēšanas veids, kurā izmanto medikamentus vai citas vielas, lai iedarbotos tieši uz noteiktiem mehānismiem vēža šūnās, pēc iespējas mazāk ietekmējot veselās šūnas. Atšķirībā no tradicionālās ķīmijterapijas, kas iedarbojas uz strauji dalīties spējīgām šūnām kopumā, mērķterapija bloķē konkrētas molekulas (piemēram, enzīmus vai olbaltumvielas), kas iesaistītas vēža šūnu augšanā un izplatībā. Tāpēc dažkārt mērķterapijai var būt mazāk vai atšķirīgas blakusparādības nekā ķīmijterapijai, taču arī tā var radīt nevēlamas reakcijas.
Visbiežāk mērķterapijas medikamenti ir:
Mērķterapijas piemērotību nosaka, balstoties uz audzēja bioloģiskajām īpašībām un īpašiem testiem.
Olnīcu vēža gadījumā mērķterapija parasti tiek lietota kombinācijā ar ķīmijterapiju, un galvenie mērķterapijas veidi ir šādi:
2023. gada janvārī publicēta klīniskā pētījuma rezultāti lasāmi: ŠEIT.
Mērķterapijas medikamenti iedarbojas uz konkrētiem šūnu proteīniem un receptoriem. Tā kā šīs molekulas piedalās arī normālu organisma funkciju regulēšanā (piemēram, asinsspiediena, ādas un zarnu darbības kontrolē), ārstēšanas laikā var rasties blakusparādības.
Blaknes daļēji var līdzināties ķīmijterapijas izraisītajām un visbiežāk ietver:
Tomēr daudzos gadījumos blakusparādības iespējams mazināt, pielāgojot zāļu devu, mainot lietošanas režīmu vai nozīmējot papildu atbalstošu terapiju. Par jebkurām sūdzībām ir svarīgi savlaicīgi informēt ārstējošo ārstu.62
Par ķīmijterapijas blaknēm vairāk lasīt: ŠEIT.

Olnīcu vēzim nav nekādu skrīninga izmeklējumu. Taču regulāras profilaktiskās vizītes pie ginekologa palielina iespēju, ka olnīcu vēzis tiks atklāts sākotnējās stadijās. Tāpēc viens no galvenajiem priekšnoteikumiem olnīcu vēža profilaksē ir regulāras ginekoloģiskās apskates, kā arī ultrasonogrāfiski izmeklējumi.

Olnīcu vēzim nav nekādu skrīninga izmeklējumu. Taču regulāras profilaktiskās vizītes pie ginekologa palielina iespēju, ka olnīcu vēzis tiks atklāts sākotnējās stadijās. Tāpēc viens no galvenajiem priekšnoteikumiem olnīcu vēža profilaksē ir regulāras ginekoloģiskās apskates, kā arī ultrasonogrāfiski izmeklējumi.
Ir vairāki veidi, kā samazināt risku saslimt ar visbiežāk sastopamo olnīcu vēža veidu – epitēlija olnīcu vēzi. Minētie profilakses paņēmieni neattiecas uz dīgļšūnu un stromālo šūnu vēzi, kuri pagaidām nav pietiekami izpētīti.
Olnīcu un olvadu izņemšana (profilaktiska operācija)
Profilaktiska olnīcu un olvadu izņemšana (risk-reducējoša salpingo-ooforektomija) būtiski samazina olnīcu vēža risku, taču to nenovērš pilnībā. Retos gadījumos līdzīgs audzējs var attīstīties vēdera dobuma gļotādā (primārs peritoneāls vēzis).
Šī operācija netiek rekomendēta visām sievietēm kā profilakses standarts, bet to var apsvērt augsta riska gadījumā, piemēram:
Svarīgi zināt, ka olnīcu izņemšana izraisa priekšlaicīgu menopauzi, kas var būt saistīta ar:
Tādēļ lēmums par profilaktisku operāciju jāpieņem rūpīgi, konsultējoties ar ginekologu, onkologu un, ja nepieciešams, ģenētikas speciālistu.64
Ir zināmi faktori, kas var samazināt biežākā – epiteliālā – olnīcu vēža risku:
Pētījumi rāda: jo vairāk ovulācijas ciklu sievietes dzīves laikā, jo lielāks var būt olnīcu vēža risks. Savukārt situācijas, kas samazina ovulāciju skaitu – piemēram, grūtniecība, zīdīšana vai hormonālā kontracepcija –, var šo risku mazināt.
Kontracepcijas tabletes – ir konstatēts, ka orālās kontracepcijas līdzekļu lietošana samazina olnīcu vēža risku par 30–50 %.65 Arvien vairāk pētījumu norāda uz uztura ietekmi olnīcu vēža riska mazināšanā. Starptautiski pētījumi liecina, ka lielāks rūpnieciski pārstrādātu un fritētu produktu patēriņš, īpaši transtaukskābju uzņemšana, var būt saistīta ar paaugstinātu olnīcu vēža risku.
Šī saistība daļēji skaidrojama ar to, ka transtaukskābes veicina aptaukošanos un hronisku iekaisumu organismā – abi šie faktori ir zināmi vēža riska palielinātāji. Tāpēc sabalansēts, daudzveidīgs uzturs ar ierobežotu pārstrādātu produktu patēriņu ir viens no svarīgiem soļiem vēža, tostarp olnīcu vēža, profilaksē.66
2020. gadā publicēts prospektīvs pētījums, viens no pirmajiem pētījumiem par taukskābju saistību ar epiteliālu olnīcu vēža risku, analizējot 1486 epiteliāla olnīcu vēža gadījumus, atklāj, ka, palielinoties trans - elaidīnskābes (cietas konsistences taukskābe, atrodama hidrogenētos augu taukos, margarīnā, fritētos produktos) patēriņam uzturā, palielinās epiteliālā olnīcu vēža risks. Dažādos epiteliāla olnīcu vēža histoloģiskajos apakštipos šīs sakarības nebija atšķirīgas.
Vairāk par pētījumu lasiet: ŠEIT.
